Ngày 6 và 7 tháng 11 vừa qua, Hội thảo GMP/ EU GMP 2025, do Hiệp hội Doanh nghiệp Dược Việt Nam (VNPCA) và Hiệp hội Kỹ thuật Dược phẩm Quốc tế - chi nhánh Singapore (ISPE Singapore) đồng tổ chức, đã diễn ra thành công rực rỡ. Sự kiện quy tụ các chuyên gia hàng đầu trong nước và quốc tế, nhằm chia sẻ các chiến lược và giải pháp thực tiễn cho cộng đồng doanh nghiệp Việt Nam.
Trong đó, bài tham luận của GMPc Việt Nam đã trở thành một điểm nhấn quan trọng, thu hút sự quan tâm đặc biệt của các đại biểu. Đại diện cho tiếng nói chuyên môn tại Việt Nam, Ông Đào Xuân Hưởng (Chủ tịch GMPc Việt Nam) đã trình bày bức tranh toàn cảnh về sự chuyển dịch tất yếu từ tư vấn WHO GMP sang EU GMP.

Không chỉ phân tích cơ hội và thách thức, phần trình bày của GMPc Việt Nam còn cung cấp một tư duy chiến lược mạch lạc, giúp các doanh nghiệp hoạch định lộ trình đầu tư hiệu quả, sẵn sàng cho hành trình vươn ra toàn cầu.

Từ Chiến lược đến Thực thi: Những Phân tích Chuyên sâu

Một trong những chủ đề được quan tâm nhất tại hội thảo là lộ trình nâng cấp EU GMP. Với vai trò là đơn vị tiên phong trong lĩnh vực tư vấn GMP/ GMP EU, Ông Đào Xuân Hưởng (Chủ tịch GMPc Việt Nam) đã đưa ra một phân tích sắc bén về "Cơ hội và Thách thức khi nâng cấp WHO GMP lên EU GMP". Dựa trên kinh nghiệm thực tiễn, ông chỉ rõ một nhận định quan trọng: việc cố gắng cải tạo một nhà máy dược phẩm thiết kế theo WHO GMP hiện hữu để đạt chuẩn EU GMP là "KHÔNG KHẢ THI".

Lý do đến từ những thách thức căn bản về kỹ thuật, đặc biệt là các rủi ro về tính toàn vẹn dữ liệu (Data Integrity) trong hệ thống cũ và chi phí cải tạo hệ thống phụ trợ (đặc biệt là vô trùng) có thể vượt cả chi phí xây mới. Từ đó, ông khẳng định chiến lược đúng đắn và hiệu quả nhất phải là "Nâng cấp đồng nghĩa xây mới" (Upgrading means building new).
Tiếp nối tầm nhìn đó, Ông Lê Ngọc Trình (Phó TGĐ Boston Pharma) đã chia sẻ "Kinh nghiệm triển khai EU GMP" thực chiến. Ông đi sâu vào việc quản trị các thách thức lớn về chi phí đầu tư (CapEx), chi phí vận hành (OpEx) và thay đổi văn hóa chất lượng (Working Culture). Việc triển khai thành công EU GMP không chỉ là tuân thủ, mà còn là chìa khóa vàng để nắm bắt cơ hội "Ưu tiên đấu thầu (Nhóm 1 & 2)" và "Hội nhập quốc tế".
Cập nhật Tiêu chuẩn Quốc tế: Từ Annex 1 đến PIC/S
Giá trị của một hội thảo EU GMP quốc tế còn nằm ở việc cập nhật các tiêu chuẩn mới nhất. Các chuyên gia hàng đầu thế giới đã mang đến những góc nhìn học thuật và kinh nghiệm thực thi quý giá.

- Bà Vee Revithi (Chuyên gia tư vấn cấp cao, Hy Lạp): Cung cấp các phân tích chi tiết về những thay đổi gần đây trong Phần 1 của Hướng dẫn EU và PIC/S GMP, đồng thời chia sẻ phương pháp làm việc hiệu quả với các cơ quan quản lý.

- Ông Bob Tribe (Cựu Chủ tịch PIC/S, Úc): Đã giải mã "Những thay đổi gần đây của Phụ lục 1 (Annex 1)"—một trong những cập nhật quan trọng và phức tạp nhất liên quan đến sản xuất vô trùng. Ông cũng chỉ ra "8 điểm yếu phổ biến nhất" mà các thanh tra viên GMP thường phát hiện, giúp doanh nghiệp chuẩn bị tốt hơn cho các cuộc đánh giá.
Giải pháp Công nghệ cho Nhà máy Dược phẩm EU GMP
Từ chiến lược đến thực thi, ngày thứ hai của hội thảo tập trung vào bộ công cụ công nghệ then chốt để vận hành một nhà máy dược phẩm EU GMP hiệu quả và tuân thủ. Các chuyên đề đã giải quyết những "điểm đau" (pain points) trong vận hành thủ công và đảm bảo tính toàn vẹn dữ liệu:

1. Chuyển đổi số (Digital Transformation): Các giải pháp số hóa toàn diện được giới thiệu bởi Factorytalk và Yokogawa Engineering Asia, giúp đảm bảo tuân thủ thông minh hơn với hệ thống eQMS và các công cụ khác.
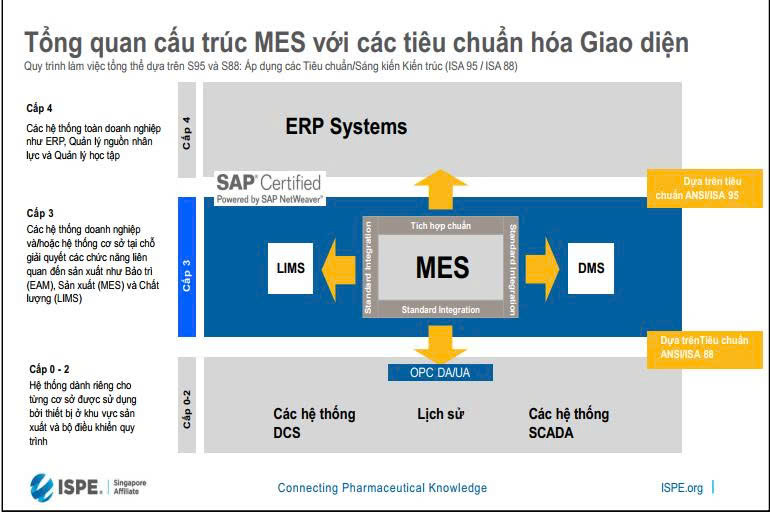
2. Hệ thống MES và EBR: Chuyên gia từ Koerber Pharma Software đã hướng dẫn cách triển khai thành công hệ thống Hồ sơ lô điện tử (EBR) và Hệ thống Điều hành Sản xuất (MES).
3. Hệ thống LIMS: Đại diện LabWare chia sẻ hướng dẫn từng bước để thay thế quy trình giấy trong phòng thí nghiệm (GLP Lab) bằng hệ thống LIMS, giải quyết bài toán cốt lõi về quản lý dữ liệu phòng thí nghiệm.
4. Kiểm soát Tạp nhiễm (CCS): Các chuyên gia từ Cytiva và STERIS đã trình bày sâu về "Chiến lược Kiểm soát Tạp nhiễm (CCS)" hiệu quả cho lọc vô trùng và các yêu cầu "Làm sạch & Khử khuẩn" theo Annex 1.
Kết luận
Hội thảo EU GMP 2025 đã khép lại thành công, hoàn thành sứ mệnh cập nhật tri thức và định hình chiến lược cho ngành sản xuất Dược. Các phiên thảo luận Q&A sôi nổi và các cơ hội kết nối giá trị đã củng cố cam kết của doanh nghiệp Việt Nam trong việc chuyển hóa thách thức thành lợi thế cạnh tranh.

Với vai trò là đơn vị tư vấn WHO GMP và EU GMP hàng đầu tại Việt Nam, chúng tôi hiểu rõ những thách thức mà doanh nghiệp đang đối mặt. Hội thảo này một lần nữa khẳng định, việc nâng cấp EU GMP là một dự án đầu tư chiến lược, đòi hỏi tầm nhìn đúng đắn ngay từ đầu.

Quý Doanh nghiệp có nhu cầu tư vấn chi tiết về lộ trình xây dựng nhà máy dược phẩm EU GMP hoặc cần hỗ trợ về các giải pháp công nghệ (MES, LIMS, CCS), vui lòng liên hệ với đội ngũ chuyên gia của GMPc để được hỗ trợ.







