Trong kỷ nguyên số hóa ngành dược phẩm, Tính toàn vẹn dữ liệu (Data Integrity) không chỉ đơn thuần là một yêu cầu kỹ thuật mà còn là nền tảng cốt lõi bảo vệ sự an toàn của bệnh nhân và uy tín pháp lý của doanh nghiệp. Việc thiếu hụt dữ liệu chính xác có thể dẫn đến những quyết định sai lầm, gây nguy hiểm cho người dùng và đối mặt với các án phạt nghiêm khắc từ các cơ quan quản lý hàng đầu như FDA (Hoa Kỳ) hay EMA (Châu Âu).
Để thiết lập tiêu chuẩn cao nhất về tính toàn vẹn dữ liệu, ngành dược thế giới dựa trên bộ nguyên tắc vàng: ALCOA và ALCOA+.
1. ALCOA: 5 Trụ cột thiết yếu của dữ liệu dược phẩm
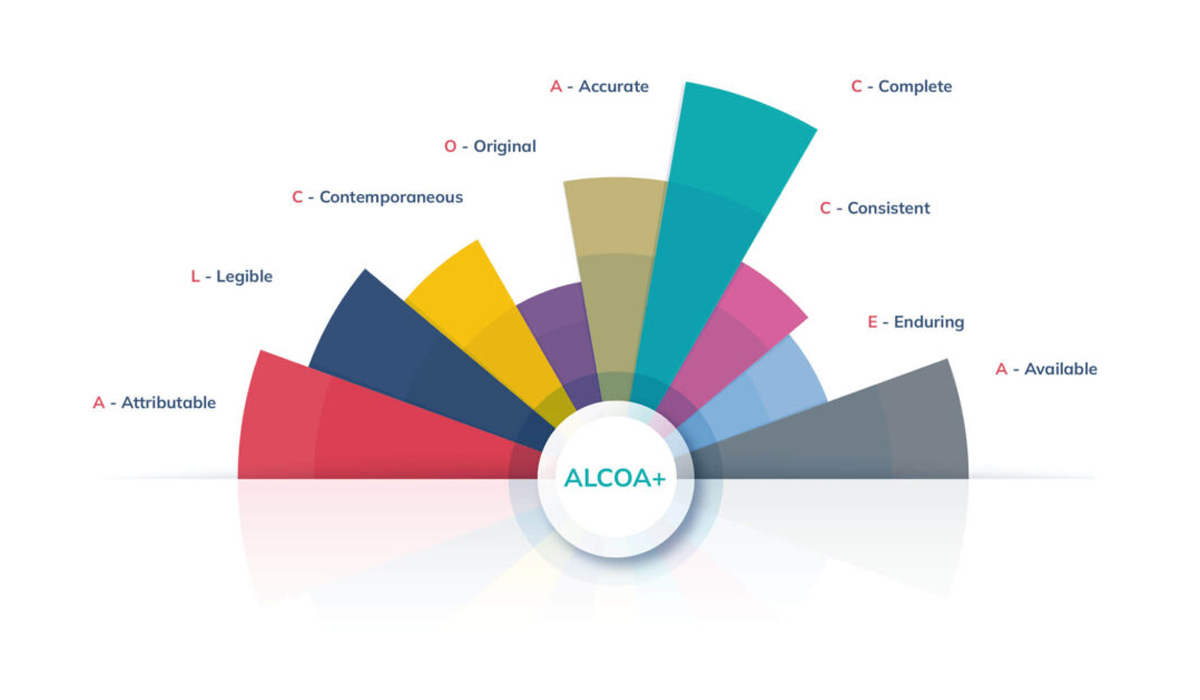
Đối với cấp quản lý và vận hành, ALCOA định nghĩa các yêu cầu tối thiểu để một dữ liệu được coi là "có giá trị pháp lý" và đáng tin cậy:
- Attributable (Có thể truy xuất): Mọi dữ liệu phải gắn liền với một cá nhân cụ thể. Việc xác định rõ người thu thập hoặc ghi chép giúp đảm bảo tính trách nhiệm, tính minh bạch và ngăn chặn các hành vi gian lận hồ sơ.
- Legible (Dễ đọc): Dữ liệu phải được ghi chép rõ ràng, dễ hiểu và tồn tại vĩnh viễn trong suốt vòng đời của nó. Điều này đảm bảo dữ liệu có thể được rà soát, giải trình và phân tích chính xác tại bất kỳ thời điểm nào trong tương lai.
- Contemporaneous (Tính thời điểm): Dữ liệu phải được ghi chép ngay tại thời điểm hoạt động diễn ra. Việc ghi chép hồi cứu (ghi sau khi sự việc đã kết thúc) là một trong những lỗi nghiêm trọng nhất dẫn đến sai lệch thông tin và bị bắt lỗi trong các kỳ thanh tra.
- Original (Tính nguyên bản): Dữ liệu phải được lưu giữ ở dạng sơ khai nhất (Raw data). Mọi thay đổi hoặc hiệu chỉnh phải được thực hiện theo quy trình, có ký xác nhận và giải trình lý do chính đáng, không được phép tẩy xóa dữ liệu gốc.
- Accurate (Chính xác): Dữ liệu phải phản ánh đúng giá trị thực tế của hoạt động sản xuất hoặc kiểm nghiệm. Đây là yếu tố sống còn để Ban lãnh đạo đưa ra các quyết định xuất xưởng sản phẩm an toàn và chất lượng.
2. ALCOA+: Mở rộng phạm vi quản trị vòng đời dữ liệu hiện đại
Để thích ứng với các hệ thống dữ liệu điện tử phức tạp và yêu cầu ngày càng khắt khe của EU GMP, bộ nguyên tắc ALCOA+ bổ sung thêm 4 yếu tố then chốt:
- Complete (Đầy đủ): Hồ sơ phải bao gồm toàn bộ thông tin liên quan, bao gồm cả các kết quả lỗi, dữ liệu thử nghiệm lại hoặc các lần phân tích bị hủy. Không được phép lựa chọn dữ liệu (Cherry-picking) để báo cáo.
- Consistent (Nhất quán): Dữ liệu phải thống nhất về định dạng, trình tự thời gian và phương pháp ghi chép trên tất cả các loại hồ sơ, từ nhật ký vận hành đến phiếu kiểm nghiệm.
- Enduring (Bền vững): Dữ liệu phải được lưu trữ an toàn trên các vật liệu hoặc hệ thống lưu trữ có độ bền cao, đi kèm với các giải pháp sao lưu (backup) và phục hồi sau sự cố để đảm bảo tính ổn định trong nhiều năm.
- Available (Sẵn có): Dữ liệu phải luôn sẵn sàng để truy cập, trích xuất và rà soát bất cứ khi nào cơ quan quản lý yêu cầu thanh tra đột xuất hoặc định kỳ.
3. Chiến lược ứng dụng ALCOA+ trong quản trị nhà máy
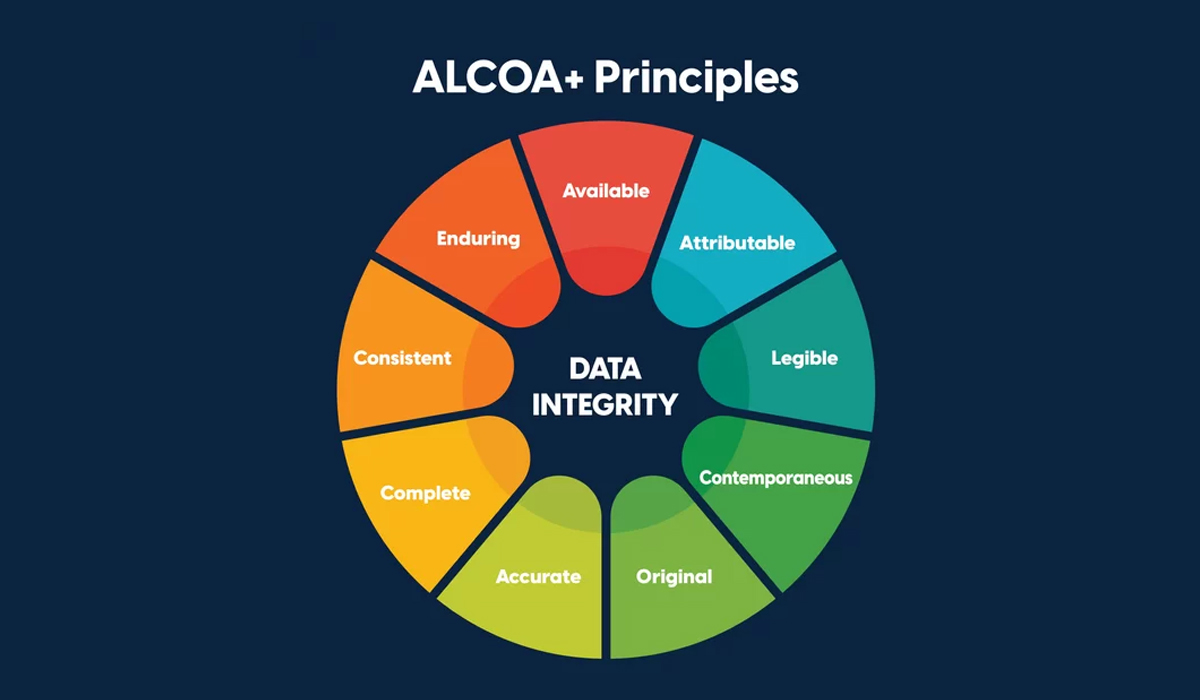
Việc áp dụng ALCOA+ thành công không chỉ nằm ở quy trình (SOP) mà cần sự phối hợp đồng bộ giữa công nghệ và văn hóa doanh nghiệp:
- Giai đoạn thu thập & Vận hành: Đào tạo nhân sự về ý thức trách nhiệm cá nhân. Mọi thao tác trên máy móc hoặc thiết bị phân tích phải được thực hiện bởi nhân viên có chuyên môn và tuân thủ tuyệt đối quy trình vận hành chuẩn.
- Hệ thống lưu trữ & Bảo mật: Đầu tư vào hạ tầng CNTT đạt chuẩn, có tính năng phân quyền truy cập (Access Control) và ghi vết thao tác (Audit Trail) để ngăn chặn việc chỉnh sửa dữ liệu trái phép.
- Kiểm soát & Phân tích: Thiết lập quy trình rà soát Audit Trail định kỳ bởi bộ phận QA. Mọi sai lệch dữ liệu phải được điều tra nguyên nhân gốc rễ và xử lý thông qua hệ thống CAPA (Hành động khắc phục và phòng ngừa).
Kết luận
Nguyên tắc ALCOA+ là thước đo uy tín của một nhà máy dược phẩm hiện đại. Việc thực thi nghiêm túc các nguyên tắc này giúp doanh nghiệp loại bỏ các rủi ro về pháp lý, tránh được các án phạt tài chính nặng nề và nguy cơ thu hồi sản phẩm.
Đối với các nhà đầu tư và quản lý, đầu tư vào tính toàn vẹn dữ liệu chính là khoản đầu tư chiến lược để bảo vệ giá trị thương hiệu và tạo dựng niềm tin bền vững trên thị trường dược phẩm quốc tế.







