Trong vòng đời thẩm định thiết bị và hệ thống (Qualification), Thẩm định thiết kế (Design Qualification - DQ) là giai đoạn khởi đầu nhưng đóng vai trò quyết định nhất đến thành công của dự án. Một sai sót nhỏ trong khâu thiết kế không được phát hiện kịp thời có thể dẫn đến những lãng phí khổng lồ về chi phí cải tạo và rủi ro không đạt chuẩn trong tương lai.
Đối với các nhà đầu tư và quản lý, DQ không chỉ là một bộ hồ sơ tuân thủ, mà là công cụ để kiểm soát chất lượng ngay từ "bản vẽ", đảm bảo thiết bị hoàn toàn phù hợp với mục đích sử dụng và các tiêu chuẩn quy định.
1. DQ là gì và tại sao Chủ đầu tư cần đặc biệt quan tâm?
Thẩm định thiết kế (DQ) là quá trình thiết lập bằng chứng bằng văn bản để xác nhận rằng thiết kế dự kiến của thiết bị, hệ thống hoặc cơ sở hạ tầng đáp ứng đầy đủ các yêu cầu của người sử dụng (URS) và các tiêu chuẩn quản lý (như EU GMP, FDA).

Tại sao DQ lại quan trọng?
- Tối ưu hóa chi phí (CAPEX): Phát hiện và khắc phục các lỗi thiết kế trước khi tiến hành chế tạo hoặc lắp đặt sẽ rẻ hơn gấp nhiều lần so với việc sửa chữa khi thiết bị đã thành hình.
- Đảm bảo tính tuân thủ: Xác nhận thiết kế tuân thủ các tiêu chuẩn vệ sinh, khả năng làm sạch và ngăn ngừa nhiễm chéo – những yếu tố sống còn trong sản xuất dược phẩm.
- Giảm thiểu rủi ro vận hành: Đảm bảo thiết bị có năng suất, độ an toàn và hiệu năng đúng như kỳ vọng ban đầu.
2. Các mục tiêu chiến lược của quá trình DQ
Một quá trình DQ bài bản phải đạt được các mục tiêu sau:
- Xác minh thiết kế đáp ứng chính xác các thông số kỹ thuật và yêu cầu chức năng.
- Nhận diện và xử lý các lỗi thiết kế tiềm ẩn có thể ảnh hưởng đến hiệu suất, an toàn hoặc chất lượng sản phẩm.
- Thiết lập hồ sơ gốc cho các hoạt động thẩm định tiếp theo (IQ, OQ, PQ) và phục vụ công tác thanh tra.
- Đảm bảo hệ thống có khả năng sản xuất ra các sản phẩm an toàn, hiệu quả và đạt chất lượng cao.
3. Lộ trình triển khai Thẩm định thiết kế tiêu chuẩn
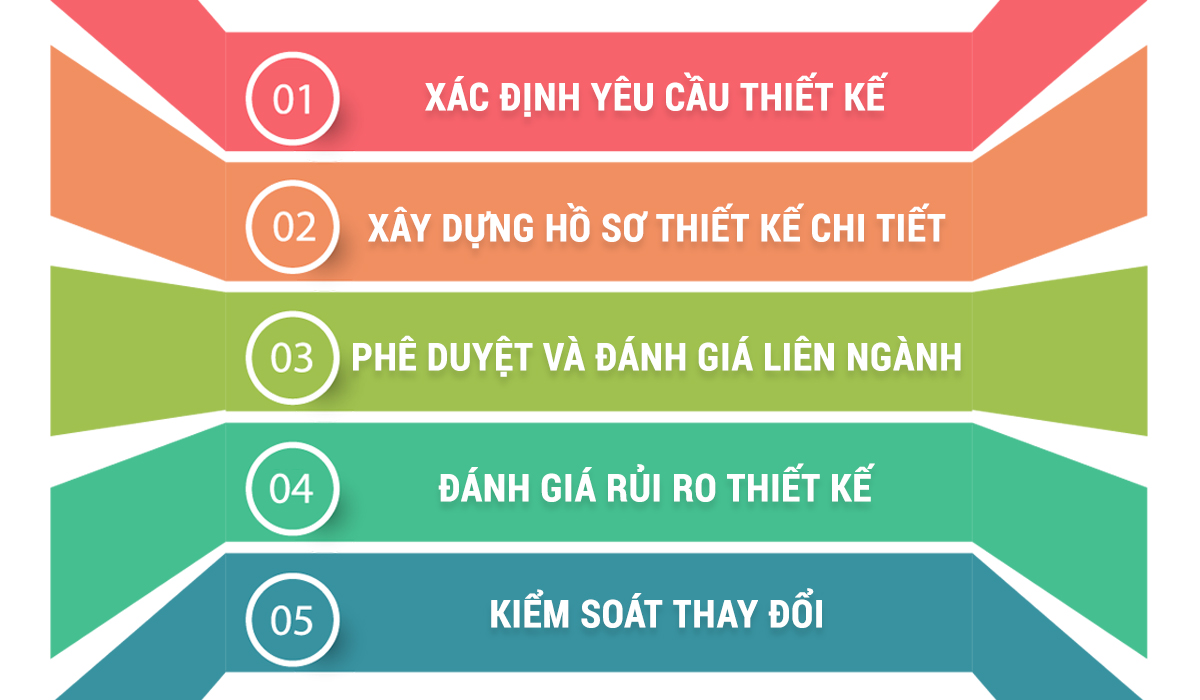
Để DQ trở thành công cụ quản trị thực thụ, quy trình triển khai cần tuân thủ các bước sau:
- Xác định yêu cầu thiết kế: Thiết lập các tiêu chí hiệu năng, tiêu chuẩn pháp lý (GMP) và mục đích sử dụng cụ thể.
- Xây dựng hồ sơ thiết kế chi tiết: Bao gồm bản vẽ kỹ thuật, thông số vật liệu, sơ đồ công nghệ (P&ID) và các tài liệu liên quan khác.
- Phê duyệt và đánh giá liên ngành: Hồ sơ thiết kế cần được rà soát bởi đội ngũ đa chức năng gồm kỹ thuật, sản xuất và đặc biệt là bộ phận Đảm bảo chất lượng (QA).
- Đánh giá rủi ro thiết kế: Sử dụng các công cụ như FMEA để nhận diện các nguy cơ tiềm ẩn liên quan đến thiết kế và đưa ra các biện pháp giảm thiểu (ví dụ: thay đổi vật liệu, bổ sung tính năng an toàn).
- Kiểm soát thay đổi (Change Control): Mọi sửa đổi trong thiết kế sau khi đã phê duyệt DQ phải được kiểm soát chặt chẽ để đảm bảo tính nhất quán và tuân thủ.
4. Góc nhìn quản trị: DQ là bảo hiểm cho hiệu quả vận hành
DQ không phải là một thủ tục hành chính rời rạc mà là một phần của quy trình xác minh và thẩm định tổng thể. Việc đầu tư nghiêm túc vào giai đoạn DQ giúp chủ doanh nghiệp:
- Rút ngắn thời gian đưa sản phẩm ra thị trường (Time-to-market): Tránh được các sự cố kỹ thuật gây chậm trễ trong giai đoạn lắp đặt và vận hành.
- Xây dựng văn hóa chất lượng: Thể hiện cam kết tuân thủ ngay từ giai đoạn đầu tư ban đầu.
Kết luận
Thẩm định thiết kế (DQ) chính là "chốt chặn" đầu tiên và quan trọng nhất để đảm bảo hệ thống và thiết bị của nhà máy dược phẩm được xây dựng đúng ngay từ đầu. Một quy trình DQ chặt chẽ không chỉ bảo vệ sự an toàn của bệnh nhân mà còn bảo vệ chính hiệu quả đầu tư của doanh nghiệp.







