Ngành công nghiệp làm đẹp tại Việt Nam đang đứng trước một ngưỡng cửa lịch sử của sự chuyển mình, nơi các giá trị truyền thống về thảo mộc kết hợp với các tiêu chuẩn sản xuất hiện đại bậc nhất thế giới. Từ một quốc gia chủ yếu tiêu thụ mỹ phẩm ngoại nhập và các cơ sở sản xuất quy mô hộ gia đình, Việt Nam đã nhanh chóng vươn lên trở thành một trong những thị trường mỹ phẩm năng động nhất khu vực Đông Nam Á. Sự chuyển dịch này không chỉ nằm ở quy mô doanh thu mà quan trọng hơn là sự nâng cấp về tư duy sản xuất: từ những xưởng sản xuất chỉ đáp ứng điều kiện cơ bản theo Nghị định 93/2016/NĐ-CP sang các nhà máy đạt tiêu chuẩn Thực hành tốt sản xuất mỹ phẩm của Hiệp hội các quốc gia Đông Nam Á (CGMP ASEAN). Báo cáo này đi sâu phân tích toàn cảnh thị trường, các rào cản pháp lý, động lực kỹ thuật và lộ trình chuyển đổi chiến lược cho các doanh nghiệp mỹ phẩm nội địa đến năm 2030.
I. Phân tích thực trạng và tiềm năng thị trường mỹ phẩm Việt Nam giai đoạn 2024 - 2033
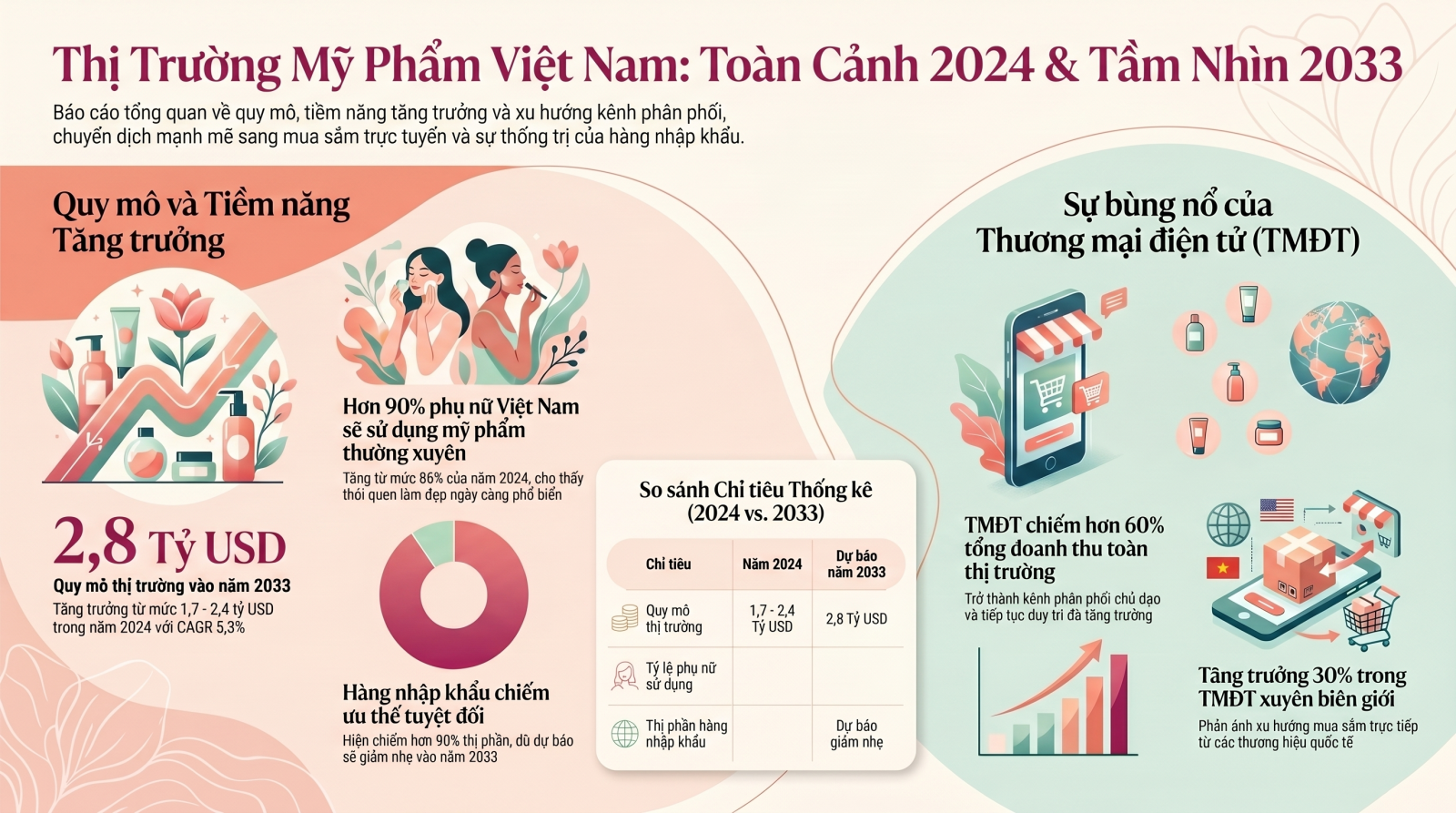
Thị trường mỹ phẩm Việt Nam ghi nhận sự tăng trưởng ổn định bất chấp những biến động kinh tế toàn cầu. Theo các số liệu thống kê từ Statista, quy mô thị trường năm 2024 ước đạt 2,4 tỷ USD, tăng 3,4% so với năm 2023. Các dự báo dài hạn hơn từ IMARC Group chỉ ra rằng thị trường có thể đạt mức 2,8 tỷ USD vào năm 2033 với tốc độ tăng trưởng kép hàng năm (CAGR) là 5,3% trong giai đoạn 2025-2033. Những con số này minh chứng cho sức mua mạnh mẽ của một quốc gia có cơ cấu dân số trẻ và tầng lớp trung lưu đang mở rộng nhanh chóng.
1. Động lực tăng trưởng và hành vi người tiêu dùng
Sự gia tăng tỷ lệ phụ nữ sử dụng các sản phẩm làm đẹp thường xuyên từ 76% (năm 2018) lên 86% (năm 2022) là minh chứng rõ nét nhất cho sự thay đổi nhận thức về chăm sóc cá nhân. Người tiêu dùng Việt Nam hiện đại không chỉ quan tâm đến giá cả mà còn đặc biệt khắt khe về nguồn gốc xuất xứ, thành phần sản phẩm và uy tín của nhà sản xuất. Điều này đặt ra áp lực lớn buộc các cơ sở sản xuất trong nước phải nâng cấp tiêu chuẩn để không bị đào thải ngay trên sân nhà.
Sự bùng nổ của các sàn thương mại điện tử như Shopee, Lazada và TikTok Shop đã thay đổi hoàn toàn cục diện phân phối, chiếm hơn 60% doanh thu toàn ngành. Đặc biệt, xu hướng thương mại điện tử xuyên biên giới với CAGR dự báo đạt 30% giai đoạn 2024-2028 đang mở ra cánh cửa cho các thương hiệu Việt xuất khẩu trực tuyến sang thị trường quốc tế, với điều kiện sản phẩm phải đáp ứng các tiêu chuẩn chứng nhận khắt khe như CGMP ASEAN hoặc ISO 22716.
2. Cơ cấu hàng nội địa và áp lực từ hàng nhập khẩu
Mặc dù có tiềm năng lớn, thị trường mỹ phẩm Việt Nam vẫn đang bị chi phối mạnh mẽ bởi các thương hiệu ngoại. Hơn 90% sản phẩm mỹ phẩm đang lưu hành tại Việt Nam là hàng nhập khẩu. Giá trị nhập khẩu liên tục tăng qua các năm, từ 790 triệu USD năm 2018 lên tới hơn 1,3 tỷ USD chỉ trong 11 tháng đầu năm 2024.
Các quốc gia cung ứng chính bao gồm Singapore (chiếm 29,2% thị phần), Hàn Quốc, Trung Quốc, Thái Lan và Mỹ. Sự thống trị của các tập đoàn đa quốc gia như L’Oreal, Unilever hay các hãng dược mỹ phẩm như La Roche-Posay buộc các doanh nghiệp nội địa phải tìm hướng đi riêng bằng cách khai thác lợi thế thảo dược bản địa và nâng cao tiêu chuẩn sản xuất để xây dựng niềm tin nơi khách hàng.
Thống kê quy mô và dự báo thị trường mỹ phẩm Việt Nam
II. Đối chiếu hệ thống tiêu chuẩn: Nghị định 93/2016/NĐ-CP và CGMP ASEAN
Tại Việt Nam, sản xuất mỹ phẩm là ngành kinh doanh có điều kiện. Việc chuyển dịch từ một xưởng sản xuất đủ điều kiện cơ bản lên nhà máy đạt chuẩn CGMP ASEAN là một cuộc cách mạng về cả quy trình, công nghệ và tư duy quản lý.
1. Cơ sở sản xuất đủ điều kiện theo Nghị định 93/2016/NĐ-CP
Đây là cấp độ tiêu chuẩn tối thiểu mà pháp luật Việt Nam yêu cầu để một cơ sở có thể hoạt động sản xuất mỹ phẩm. Các xưởng này thường có quy mô nhỏ (tối thiểu 300m2), ngân sách đầu tư thấp (khoảng 3-10 tỷ đồng) và quy trình sản xuất đơn giản. Việc thẩm định và cấp phép do Sở Y tế địa phương thực hiện. Tuy nhiên, các cơ sở này chỉ được phép lưu hành sản phẩm trong nước và đối mặt với rủi ro phải đóng cửa hoặc nâng cấp khi các quy định về an toàn sản phẩm ngày càng trở nên nghiêm ngặt hơn.
2. Nhà máy đạt tiêu chuẩn CGMP ASEAN
CGMP ASEAN là viết tắt của "Cosmetic Good Manufacturing Practices" - bộ hướng dẫn thực hành tốt sản xuất mỹ phẩm được Hội đồng mỹ phẩm ASEAN thông qua. Đây là tiêu chuẩn mang tính khu vực, giúp sản phẩm không chỉ được lưu hành rộng rãi tại 10 nước thành viên ASEAN mà còn là bảo chứng chất lượng cho việc xuất khẩu sang các thị trường khó tính như Mỹ hay Châu Âu. Nhà máy CGMP ASEAN đòi hỏi quy mô lớn hơn (tối thiểu 500m2), vốn đầu tư cao (thường trên 10 tỷ đồng) và phải được Cục Quản lý Dược - Bộ Y tế trực tiếp thẩm định và cấp chứng nhận.
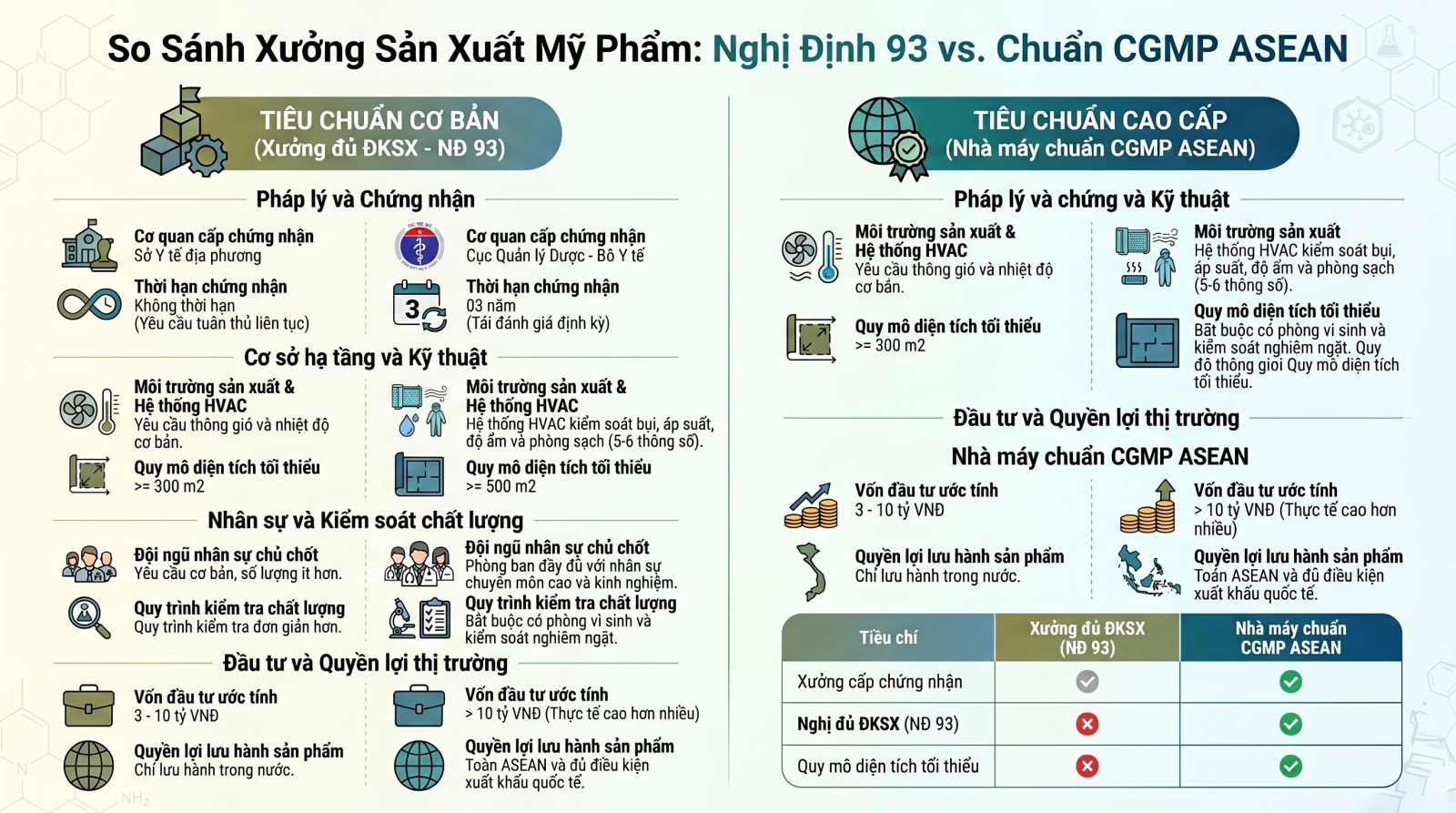
So sánh chi tiết Xưởng đủ điều kiện (NĐ 93) và Nhà máy CGMP ASEAN
III. Tác động của Dự thảo Nghị định Quản lý Mỹ phẩm (2026) đến thị trường
Dự thảo Nghị định Quản lý Mỹ phẩm mới đánh dấu một bước ngoặt lớn trong việc siết chặt quản lý chất lượng và đẩy nhanh quá trình đồng bộ hóa với tiêu chuẩn khu vực. Các điểm đáng chú ý bao gồm:
- Lộ trình bắt buộc áp dụng chuẩn CGMP: Điểm quan trọng nhất của dự thảo là yêu cầu từ ngày 01 tháng 01 năm 2028, toàn bộ các cơ sở sản xuất mỹ phẩm đang hoạt động theo Nghị định 93/2016/NĐ-CP phải đáp ứng các điều kiện sản xuất mới theo chuẩn CGMP. Điều này có nghĩa là các xưởng quy mô nhỏ chỉ đạt điều kiện cơ bản sẽ buộc phải nâng cấp hoặc đối mặt với nguy cơ bị đào thải.
- Siết chặt điều kiện nhân sự chuyên môn: Dự thảo yêu cầu người phụ trách sản xuất và người phụ trách chất lượng phải có trình độ từ đại học trở lên thuộc các chuyên ngành hóa học, sinh học, hoặc dược học, có ít nhất 02 năm kinh nghiệm và hoạt động độc lập với nhau.
- Quản lý chặt chẽ Hồ sơ thông tin sản phẩm (PIF): Cơ sở công bố phải lưu giữ PIF tối thiểu 05 năm kể từ khi lô sản xuất cuối cùng ra thị trường và phải xuất trình khi cơ quan chức năng yêu cầu.
- Kiểm nghiệm bắt buộc với các nhóm sản phẩm nhạy cảm: Đối với các sản phẩm làm trắng da, phấn rôm, chống nắng, mỹ phẩm cho phụ nữ có thai hoặc trẻ em, doanh nghiệp phải gửi mẫu đến cơ sở kiểm nghiệm độc lập đạt chuẩn (GLP hoặc ISO/IEC 17025) để kiểm tra chất lượng trong vòng 30 ngày kể từ khi lưu thông.
- Quy định nghiêm ngặt về giới hạn an toàn: Sản phẩm phải đáp ứng tuyệt đối các yêu cầu của ASEAN về giới hạn kim loại nặng (thủy ngân, asen, chì, cadimi), vi sinh vật, tạp chất và nồng độ các chất cấm.
Xem thêm: Toàn văn dự thảo Nghị định quản lý mỹ phẩm 2026
IV. Khuyến nghị chiến lược dành cho chủ đầu tư
Sự chuyển dịch từ xưởng đủ điều kiện lên CGMP ASEAN không còn là lựa chọn "có thì tốt", mà là yêu cầu bắt buộc để doanh nghiệp tồn tại và phát triển bền vững. Dựa trên thực trạng thị trường và các quy định pháp lý sắp ban hành, dưới đây là các khuyến nghị trọng tâm dành cho chủ đầu tư:
1. Đối với các chủ đầu tư đang có ý định xây mới hoặc nâng cấp nhà máy
- Hành động ngay cho lộ trình 2028: Với thời gian thẩm định và thi công một nhà máy CGMP kéo dài từ 5 đến 18 tháng, các chủ đầu tư đang vận hành theo cơ sở Nghị định 93 cần bắt tay ngay vào việc lập dự án nâng cấp để không bị gián đoạn sản xuất khi quy định mới có hiệu lực vào năm 2028.
- Xác định rõ phân khúc và lựa chọn đơn vị tư vấn sớm: Cần xác định chính xác dạng sản phẩm mục tiêu và phân khúc khách hàng ngay từ đầu để định hình công nghệ. Việc hợp tác với các đơn vị tư vấn chuyên nghiệp ngay từ giai đoạn ý tưởng có thể giúp chủ đầu tư tiết kiệm từ 20-30% chi phí đầu tư nhờ tối ưu hóa diện tích nhà xưởng và lựa chọn đúng thiết bị.
- Chuẩn bị nguồn vốn vững chắc: Đầu tư nhà máy CGMP đòi hỏi ngân sách lớn cho hệ thống phòng sạch, thiết bị chân không, và hệ thống kiểm soát môi trường (HVAC). Mức đầu tư thấp nhất cũng từ 8-12 tỷ VNĐ cho quy mô nhỏ (500m2) và có thể lên trên 40 tỷ VNĐ cho quy mô lớn.
2. Đối với các nhà máy đã đạt chuẩn CGMP ASEAN
- Chú trọng nguồn nhân lực QA/QC: Đừng coi CGMP là một đích đến, mà hãy xem đó là quá trình liên tục. Cần đầu tư đào tạo đội ngũ nhân sự quản lý chất lượng (QA/QC) trình độ cao để kiểm soát quy trình, ghi chép hồ sơ (PIF) và bảo trì thiết bị, tránh nguy cơ bị thu hồi chứng nhận trong các đợt hậu kiểm.
- Chủ động với công tác giám sát hậu mại: Xây dựng quy trình xử lý khiếu nại và thu hồi sản phẩm nhanh chóng, đặc biệt chú ý đến việc lấy mẫu kiểm nghiệm và gửi báo cáo cho Bộ Y tế khi có các biến cố bất lợi nghiêm trọng.
3. Định hướng phát triển sản phẩm tương lai
- Đón đầu xu hướng "Mỹ phẩm Xanh": Người tiêu dùng và xu hướng toàn cầu đang dịch chuyển sang các sản phẩm thuần chay (Vegan), không thử nghiệm trên động vật và mô hình sản xuất giảm phát thải (Net Zero). Tối ưu hóa năng lượng và sử dụng bao bì tái chế sẽ là lợi thế cạnh tranh lớn.
- Tận dụng lợi thế bản địa kết hợp công nghệ cao: Ưu tiên ứng dụng công nghệ sinh học và công nghệ Nano để chiết xuất hoạt chất từ thảo dược Việt Nam, tạo ra các dòng dược mỹ phẩm điều trị chuyên sâu có khả năng cạnh tranh với các thương hiệu ngoại nhập.
Phân tích chuyên sâu: Sự chuyển dịch từ Thông tư 06/2011/TT-BYT sang Nghị định quản lý mỹ phẩm mới
So sánh dự thảo Nghị định quản lý mỹ phẩm 2026 và Thông tư 06/2011/TT-BYT







