Ngành công nghiệp dược phẩm Việt Nam đang đứng trước một bước ngoặt mang tính thời đại, chuyển mình từ một nền sản xuất thuốc generic quy mô nhỏ và phân tán sang một hệ sinh thái sản xuất hiện đại, định hướng tiêu chuẩn quốc tế và hội nhập sâu rộng vào chuỗi cung ứng toàn cầu. Sự chuyển dịch này không chỉ là kết quả của các nỗ lực tự thân từ phía doanh nghiệp mà còn là hệ quả tất yếu từ những thay đổi căn bản trong khung pháp lý, dòng vốn đầu tư trực tiếp nước ngoài (FDI) và những đòi hỏi ngày càng khắt khe về chất lượng điều trị trong bối cảnh già hóa dân số nhanh chóng. Từ góc độ của một nhà nghiên cứu thị trường lâu năm, việc phân tích thực trạng sản xuất và dự báo xu hướng vận hành nhà máy đến năm 2030 đòi hỏi một cái nhìn đa chiều, kết hợp giữa các chỉ số kinh tế vĩ mô, các động lực chính sách và sự biến đổi trong cấu trúc quản trị tại các doanh nghiệp đầu ngành.
Tổng quan bức tranh thị trường và động lực tăng trưởng vĩ mô
Thị trường dược phẩm Việt Nam đã chứng kiến sự tăng trưởng vượt bậc trong gần một thập kỷ qua. Quy mô thị trường từ mức 3,4 tỷ USD vào năm 2015 đã tăng lên gần 7 tỷ USD vào năm 2023. Theo các báo cáo triển vọng kinh tế, giá trị thị trường có khả năng chạm mốc 10 tỷ USD vào năm 2026 và tiếp tục mở rộng mạnh mẽ trong giai đoạn 2027-2030. Sự tăng trưởng này được củng cố bởi bốn trụ cột chính: tốc độ tăng trưởng kinh tế ổn định, sự gia tăng nhanh chóng của thu nhập bình quân đầu người, nhận thức về sức khỏe của người dân và xu hướng nhân khẩu học không thể đảo ngược.
Về kinh tế, Việt Nam duy trì mục tiêu tăng trưởng GDP ở mức 6,5-7% trong giai đoạn 2024-2025 và dự kiến tiếp tục chu kỳ tăng trưởng mới đến năm 2030. Thu nhập bình quân đầu người dự kiến tăng từ 4.300 USD năm 2023 lên 4.900 USD năm 2025, tạo điều kiện cho người dân nâng cao khả năng chi trả cho các dịch vụ chăm sóc sức khỏe chất lượng cao. Đồng thời, chi tiêu y tế tổng thể được dự báo sẽ tăng từ 24,7 tỷ USD năm 2024 lên tới 57,1 tỷ USD vào năm 2029. Tỷ lệ chi tiêu y tế so với thu nhập khả dụng cũng đang có xu hướng gia tăng liên tục, phản ánh sự ưu tiên của hộ gia đình đối với sức khỏe trong bối cảnh gánh nặng bệnh tật thay đổi.
Về nhân khẩu học, Việt Nam đang trải qua giai đoạn già hóa dân số nhanh nhất thế giới. Năm 2023, số người từ 60 tuổi trở lên chiếm 13,9% và con số này được dự báo sẽ tăng lên hơn 25% vào năm 2050. Việt Nam dự kiến sẽ bước vào thời kỳ dân số già vào năm 2036, tạo áp lực lớn lên hệ thống y tế nhưng đồng thời cũng mở ra dư địa khổng lồ cho các nhà máy sản xuất thuốc điều trị các bệnh mãn tính như tim mạch, tiểu đường và ung thư.
Bảng 1: Dự báo các chỉ số tăng trưởng thị trường dược phẩm và y tế (2024-2030)
Hệ thống chính sách và chiến lược quốc gia: Kim chỉ nam cho sự phát triển
Sự phát triển của ngành công nghiệp dược không thể tách rời vai trò định hướng của Chính phủ. Quyết định số 376/QĐ-TTg và Quyết định số 1165/QĐ-TTg phê duyệt Chiến lược phát triển ngành Dược đến năm 2030 và tầm nhìn đến năm 2045 đã thiết lập những mục tiêu cụ thể và tham vọng. Chính phủ đặt mục tiêu xây dựng ngành dược Việt Nam ngang tầm các nước tiên tiến trong khu vực, với giá trị thị trường nằm trong tốp 3 ASEAN.
Mục tiêu cốt lõi của chiến lược là tự chủ nguồn cung thuốc nội địa, phấn đấu thuốc sản xuất trong nước đáp ứng khoảng 80% số lượng sử dụng và chiếm 70% giá trị thị trường vào năm 2030. Đây là một thách thức lớn khi hiện tại giá trị thuốc nội trúng thầu tại các bệnh viện mới chỉ chiếm hơn 26%. Để hiện thực hóa điều này, Chính phủ đã triển khai hàng loạt ưu đãi đầu tư, từ thủ tục hành chính đến hỗ trợ tài chính cho các dự án sản xuất thuốc biệt dược gốc, thuốc phát minh, vaccine và sinh phẩm y tế.
Luật Đấu thầu năm 2023, có hiệu lực từ ngày 01/01/2024, đã tạo ra một "cú hích" trực tiếp cho các nhà máy sản xuất thuốc nội. Quy định mới ưu tiên tuyệt đối thuốc sản xuất trong nước tại các gói thầu bệnh viện nếu có ít nhất 3 hãng nội địa đáp ứng tiêu chí kỹ thuật, chất lượng và giá cả. Đặc biệt, Thông tư 03/2024/TT-BYT đã ban hành danh mục 93 hoạt chất có ít nhất 3 hãng trong nước sản xuất trên dây chuyền đạt chuẩn EU GMP hoặc tương đương, buộc các bệnh viện công lập phải ưu tiên mua sắm thuốc nội thay vì thuốc nhập khẩu có cùng tiêu chí kỹ thuật. Điều này không chỉ giúp gia tăng thị phần cho thuốc nội mà còn thúc đẩy các doanh nghiệp phải không ngừng nâng cao tiêu chuẩn sản xuất để có tên trong danh mục ưu đãi này.
Cuộc đua nâng cấp tiêu chuẩn sản xuất: EU GMP và Japan GMP
Trong thập kỷ trước, tiêu chuẩn WHO GMP là đích đến của hầu hết các nhà máy dược phẩm tại Việt Nam. Tuy nhiên, trong bối cảnh hội nhập hiện nay, WHO GMP chỉ còn là tiêu chuẩn tối thiểu để duy trì hoạt động. Các doanh nghiệp đầu ngành đã nhận thức rõ rằng, để cạnh tranh sòng phẳng với thuốc ngoại nhập tại kênh ETC (đấu thầu bệnh viện) và hướng tới xuất khẩu, việc sở hữu các dây chuyền đạt chuẩn EU GMP, Japan GMP hoặc PIC/S GMP là yêu cầu bắt buộc.
Tiêu chuẩn EU GMP (Thực hành tốt sản xuất thuốc theo tiêu chuẩn Châu Âu) đòi hỏi mức độ đầu tư cực lớn, thường lên đến hàng trăm tỷ, thậm chí hàng nghìn tỷ đồng cho mỗi dây chuyền sản xuất. Chi phí này bao gồm hạ tầng nhà xưởng hiện đại, hệ thống kiểm soát môi trường (HVAC) khắt khe, trang thiết bị tự động hóa cao và chi phí vận hành, thẩm định nghiêm ngặt. Tuy nhiên, đổi lại, các sản phẩm ra đời từ nhà máy EU-GMP sẽ được xếp vào Nhóm 1 hoặc Nhóm 2 trong đấu thầu, nơi có giá trúng thầu tốt hơn và ít bị cạnh tranh bởi các sản phẩm giá rẻ.
Theo các số liệu cập nhật, Việt Nam hiện có khoảng 18 doanh nghiệp đạt tiêu chuẩn EU-GMP hoặc Japan-GMP và con số này dự kiến sẽ tăng nhanh trong giai đoạn 2025-2030 nhằm đạt mục tiêu 20% cơ sở sản xuất đạt chuẩn cao theo Chiến lược quốc gia. Các doanh nghiệp tiên phong như Imexpharm (IMP), Dược Hậu Giang (DHG), Pymepharco (Stada) và Bidiphar (DBD) đang dẫn đầu xu hướng này bằng việc liên tục khởi công và khánh thành các cụm nhà máy tiêu chuẩn cao.
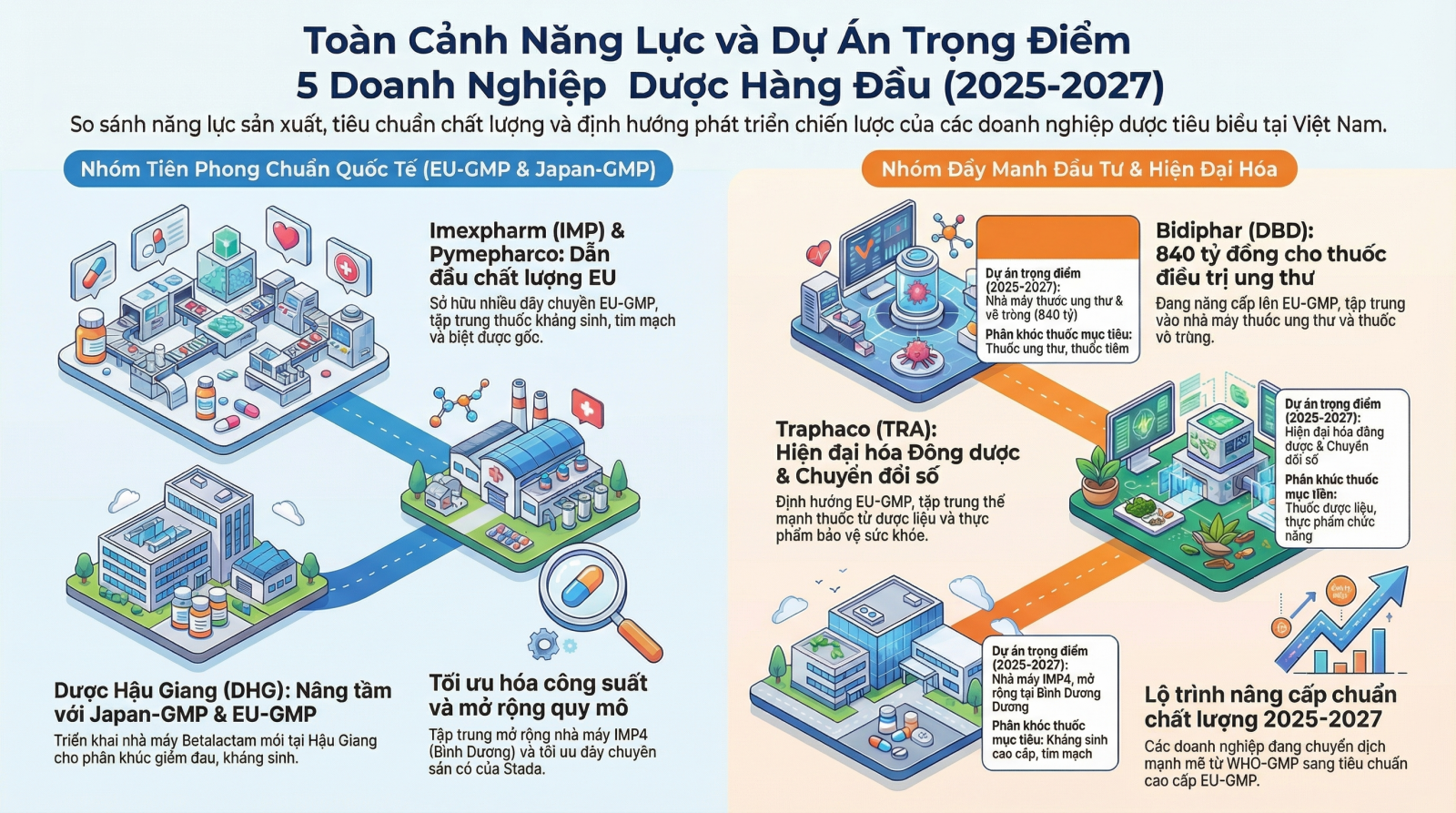
Bảng 2: Phân tích năng lực và dự án trọng điểm của các doanh nghiệp dược tiêu biểu
Phân tích sâu hơn vào trường hợp của Bidiphar, việc đầu tư 840 tỷ đồng cho nhà máy sản xuất thuốc vô trùng tại Bình Định là một minh chứng cho chiến lược tập trung vào phân khúc khó. Dự án này dự kiến hoàn tất lắp đặt thiết bị vào cuối năm 2025 và bắt đầu vận hành sau khi được cấp phép vào năm 2027. Mục tiêu đạt chuẩn EU GMP vào năm 2028 cho thấy lộ trình bài bản của doanh nghiệp: từ xây dựng cơ bản đến đạt chuẩn WHO và cuối cùng là hoàn thiện các yêu cầu khắt khe của EU. Với công suất 120 triệu sản phẩm/năm, nhà máy này sẽ giúp Bidiphar củng cố vị thế dẫn đầu trong mảng thuốc ung thư và thuốc tiêm tại Việt Nam.
Chuyển đổi số và Nhà máy thông minh: Xu hướng vận hành tất yếu đến năm 2030
Đến năm 2030, hiệu quả vận hành của một nhà máy dược phẩm không còn chỉ được đo bằng quy mô nhà xưởng mà nằm ở mức độ ứng dụng công nghệ số. Chuyển đổi số trong ngành dược tại Việt Nam đang chuyển dịch từ giai đoạn "số hóa tài liệu" sang giai đoạn "vận hành thông minh" (Smart Factory).
Các giải pháp như ERP (Quản trị nguồn lực doanh nghiệp), MES (Hệ thống điều hành sản xuất) và LIMS (Hệ thống quản lý thông tin phòng thí nghiệm) đang dần trở thành tiêu chuẩn chung. Traphaco là một ví dụ điển hình khi hợp tác với FPT Digital để thực hiện lộ trình chuyển đổi số đến năm 2025 và định hướng 2030, tập trung vào 6 hạng mục lớn với 139 tiêu chí đánh giá mức độ trưởng thành số. Việc chuyển đổi này giúp doanh nghiệp tối ưu hóa quy trình sản xuất, kiểm soát chất lượng nghiêm ngặt và đặc biệt là nâng cao khả năng truy xuất nguồn gốc sản phẩm.
Vai trò của Trí tuệ nhân tạo (AI) và Internet vạn vật (IoT) cũng đang bắt đầu len lỏi vào các khâu nghiên cứu và sản xuất. AI giúp rút ngắn quy trình sàng lọc hợp chất và tối ưu hóa công thức thuốc, giảm thiểu thời gian và chi phí R&D. IoT được ứng dụng trong việc giám sát tự động các điều kiện môi trường phòng sạch, kho bảo quản và theo dõi hành trình thuốc trong chuỗi cung ứng, đảm bảo chất lượng thuốc đến tay người bệnh không bị biến đổi. Sự kết hợp này không chỉ giúp doanh nghiệp tăng sức cạnh tranh mà còn đáp ứng các yêu cầu về tính minh bạch dữ liệu (Data Integrity) trong các đợt thanh tra GMP của quốc tế.
Mô hình Khu công nghiệp Dược phẩm chuyên biệt: Bước đột phá về hạ tầng
Một trong những xu hướng quan trọng nhất trong vận hành nhà máy đến năm 2030 là sự tập trung hóa vào các Khu công nghiệp (KCN) dược phẩm chuyên biệt. Thay vì các nhà máy nằm rải rác, việc tập trung vào một hệ sinh thái giúp các doanh nghiệp chia sẻ hạ tầng dùng chung, tối ưu hóa hệ thống xử lý chất thải và thu hút đầu tư FDI hiệu quả hơn.
Dự án KCN Dược – Sinh học Thái Bình tại huyện Quỳnh Phụ là dự án tiên phong và quy mô nhất hiện nay với diện tích hơn 292 ha và tổng vốn đầu tư hạ tầng dự kiến 3.800 tỷ đồng. Đây được coi là KCN dược phẩm hiện đại và đồng bộ đầu tiên tại Việt Nam, tích hợp đầy đủ các viện nghiên cứu, khu công nghệ sinh học, trung tâm logistics và khu nhà ở cho chuyên gia. Mục tiêu thu hút đầu tư 2 tỷ USD vào khu vực này trong giai đoạn từ nay đến năm 2030 cho thấy tầm vóc của một trung tâm sản xuất dược phẩm khu vực. Các sản phẩm sản xuất tại đây dự kiến sẽ được hưởng các ưu đãi đặc biệt về thuế và ưu tiên trong đấu thầu, tạo ra một lợi thế cạnh tranh áp đảo cho các doanh nghiệp đặt cơ sở sản xuất tại đây.
Mô hình này cũng đang được nghiên cứu triển khai tại các tỉnh miền Nam như Long An (dự án Tandoland 250 ha) hoặc các tỉnh miền Trung, nhằm hình thành các cực tăng trưởng dược phẩm trọng điểm trên khắp cả nước. Việc tập trung hóa không chỉ giúp giảm chi phí đầu tư ban đầu cho doanh nghiệp mà còn tạo điều kiện thuận lợi cho việc chuyển giao công nghệ từ các tập đoàn đa quốc gia.
Bài toán tự chủ nguyên liệu (API) và rủi ro chuỗi cung ứng
Một "gót chân Achilles" của ngành dược Việt Nam hiện nay là sự phụ thuộc quá lớn vào nguồn nguyên liệu nhập khẩu. Khoảng 90% nguyên liệu sản xuất thuốc (API) phải nhập từ Trung Quốc và Ấn Độ. Sự phụ thuộc này đã bộc lộ những rủi ro cực lớn trong giai đoạn đại dịch COVID-19, khi chuỗi cung ứng bị đứt gãy và giá nguyên liệu biến động khó lường.
Chiến lược quốc gia đặt mục tiêu đến năm 2030 tự chủ sản xuất được 20-30% nhu cầu nguyên liệu. Tuy nhiên, việc sản xuất API đòi hỏi trình độ hóa dầu và hóa dược rất cao, kèm theo các yêu cầu khắt khe về bảo vệ môi trường. Hiện tại, cả nước chỉ có 6 doanh nghiệp đăng ký sản xuất hóa dược, và sản phẩm chủ yếu là các hoạt chất đơn giản như Magie cacbonat hay Canxi photphat.
Để giải quyết bài toán này, Chính phủ đang khuyến khích các dự án đầu tư sản xuất nguyên liệu cho các nhóm thuốc thiết yếu như kháng sinh, thuốc giảm đau và các loại vitamin. Xu hướng phát triển API sinh học cũng được coi là một hướng đi đột phá, giúp Việt Nam thoát khỏi sự phụ thuộc vào các hoạt chất hóa học truyền thống và đón đầu kỷ nguyên sinh dược học. Tầm nhìn đến năm 2040 là tự chủ được 30-40% API sinh học quan trọng, đưa Việt Nam trở thành trung tâm sản xuất thuốc sinh học của khu vực ASEAN.
Tác động của M&A và FDI đến tiêu chuẩn quản trị và công nghệ
Làn sóng M&A (Mua bán và Sáp nhập) trong ngành dược Việt Nam đang diễn ra mạnh mẽ hơn bao giờ hết, góp phần tái cấu trúc lại năng lực sản xuất của toàn ngành. Việc các tập đoàn đa quốc gia nắm giữ cổ phần chi phối tại các doanh nghiệp nội địa đã mang lại một "luồng gió mới" về tiêu chuẩn quản trị và công nghệ.
Sự hiện diện của Abbott tại Domesco, Stada tại Pymepharco, Taisho tại Dược Hậu Giang hay SK Group tại Imexpharm đã giúp các doanh nghiệp này nhanh chóng tiệm cận các tiêu chuẩn quản trị toàn cầu. Các đối tác ngoại mang theo quy trình kiểm soát chất lượng nghiêm ngặt, chiến lược R&D bài bản và đặc biệt là cơ hội chuyển giao công nghệ sản xuất các loại thuốc biệt dược gốc mà Việt Nam chưa sản xuất được. Dự kiến đến năm 2030, sẽ có ít nhất 100 loại thuốc biệt dược gốc và sinh phẩm được chuyển giao công nghệ sản xuất tại Việt Nam, giúp giảm gánh nặng chi phí nhập khẩu cho ngân sách y tế.
Sự tham gia của dòng vốn FDI cũng thúc đẩy tính minh bạch và chuyên nghiệp trong báo cáo tài chính cũng như thực hành ESG (Môi trường, Xã hội và Quản trị). Đây là một yếu tố then chốt để các doanh nghiệp dược Việt Nam có thể thu hút vốn từ các tổ chức tài chính quốc tế và tham gia vào chuỗi cung ứng của các tập đoàn dược phẩm hàng đầu thế giới.
ESG và Sản xuất xanh: Thước đo mới cho sự phát triển bền vững
Đến năm 2030, việc tuân thủ các tiêu chuẩn ESG sẽ không còn là hoạt động tự nguyện mà trở thành "tấm hộ chiếu" để doanh nghiệp thâm nhập vào các thị trường khó tính như EU hay Mỹ. Các nhà máy dược phẩm đang phải đối mặt với áp lực ngày càng tăng về việc giảm phát thải khí nhà kính, quản lý rác thải nguy hại và tối ưu hóa sử dụng tài nguyên nước.
Các doanh nghiệp tiên phong như Imexpharm đã đầu tư mạnh vào công nghệ xanh và quy trình sản xuất đạt chuẩn EU GMP để vừa nâng cao chất lượng sản phẩm vừa giảm tác động môi trường. OPC đã triển khai mô hình sản xuất tuần hoàn và tạo sinh kế bền vững cho cộng đồng yếu thế thông qua chuỗi cung ứng dược liệu. Việc công bố báo cáo phát triển bền vững theo chuẩn GRI đang dần trở thành xu hướng tại các doanh nghiệp niêm yết như DHG Pharma hay Domesco, giúp tăng cường uy tín và vị thế của doanh nghiệp trên thị trường vốn.
Thách thức về nguồn nhân lực trình độ cao
Một trong những rào cản lớn nhất đối với việc vận hành các nhà máy tiêu chuẩn EU GMP và Smart Factory đến năm 2030 là sự thiếu hụt nhân lực chất lượng cao. Các vị trí như Dược sĩ chuyên trách về QA, QC, chuyên gia thẩm định và kỹ sư vận hành hệ thống tự động hóa đang ở tình trạng cung không đủ cầu.
Các tiêu chuẩn quốc tế như EU GMP đòi hỏi nhân sự không chỉ có bằng cấp chuyên môn mà còn phải có kinh nghiệm thực hành thực tế tối thiểu từ 3-5 năm tại các vị trí tương đương. Sự thiếu đồng bộ giữa cơ sở đào tạo và nhu cầu của doanh nghiệp đang tạo ra những khó khăn trong việc chuyển giao công nghệ. Để giải quyết vấn đề này, Chính phủ đã phê duyệt Đề án đào tạo nguồn nhân lực phục vụ phát triển công nghệ cao, tập trung vào khối ngành STEM, trí tuệ nhân tạo và công nghệ sinh học. Việc tăng cường hợp tác giữa các trường đại học y dược và doanh nghiệp trong các chương trình đào tạo tài năng sẽ là chìa khóa để cung ứng nguồn nhân lực vận hành các nhà máy hiện đại trong tương lai.
Phân tích triển vọng kinh tế và hiệu quả đầu tư
Dưới góc độ tài chính, đầu tư vào các nhà máy đạt tiêu chuẩn cao là một chiến lược "đau đớn ngắn hạn nhưng ngọt ngào dài hạn". Mặc dù chi phí khấu hao và chi phí vận hành ban đầu rất lớn, gây áp lực lên biên lợi nhuận trong 2-3 năm đầu, nhưng các doanh nghiệp này sẽ có dư địa tăng trưởng vượt trội khi thuốc nội dần thay thế thuốc ngoại ở phân khúc giá trị cao.
Năm 2024 ghi nhận sự phân hóa rõ rệt về kết quả kinh doanh giữa các doanh nghiệp dược. Trong khi các đơn vị lớn như DHG, DBD và IMP đạt kết quả tích cực nhờ đẩy mạnh mảng tự sản xuất và khai thác tốt kênh ETC, thì một số đơn vị vẫn phụ thuộc vào thương mại hoặc sản phẩm truyền thống ghi nhận lợi nhuận sụt giảm do giá vốn tăng cao. Dự báo đến năm 2030, sự phân hóa này sẽ càng trở nên gay gắt hơn. Những doanh nghiệp sở hữu hạ tầng sản xuất hiện đại và khả năng quản trị chi phí tốt sẽ trở thành các "cỗ máy in tiền", trong khi các đơn vị chậm chân trong cuộc đua công nghệ sẽ bị đào thải hoặc bị thâu tóm qua các hoạt động M&A.
Bảng 3: So sánh mục tiêu và hiệu quả dự kiến của các nhà máy dược phẩm chuẩn cao
Kết luận và Khuyến nghị chiến lược cho năm 2030
Ngành sản xuất dược phẩm Việt Nam đang bước vào một kỷ nguyên mới của sự chuyên nghiệp và hiện đại hóa. Đến năm 2030, diện mạo của ngành sẽ được định nghĩa bởi các cụm nhà máy thông minh, các khu công nghiệp chuyên biệt và sự tự chủ ngày càng cao về công nghệ cũng như nguyên liệu.
Để thành công trong giai đoạn này, các doanh nghiệp cần thực hiện các chiến lược trọng tâm:
1. Kiên định với tiêu chuẩn chất lượng cao: Việc đạt EU GMP không còn là lựa chọn mà là điều kiện sinh tồn để tiếp cận các phân khúc thuốc giá trị cao tại bệnh viện.
2. Đầu tư cho công nghệ số: Chuyển đổi số phải được thực hiện thực chất, từ khâu quản trị sản xuất đến phân phối và Marketing, nhằm tối ưu hóa chi phí và tăng tính minh bạch.
3. Tập trung vào R&D và Chuyển giao công nghệ: Thay vì chỉ sản xuất các thuốc generic thông thường, cần tập trung vào các dạng bào chế khó, thuốc đặc trị và thuốc sinh học tương tự để đón đầu nhu cầu của thị trường.
4. Chủ động chuỗi cung ứng: Tăng cường liên kết để sản xuất nguyên liệu nội địa và đa dạng hóa nguồn cung API để giảm thiểu rủi ro từ các biến động bên ngoài.
5. Thực hành quản trị bền vững (ESG): Xây dựng hình ảnh doanh nghiệp xanh và trách nhiệm xã hội để thu hút vốn ngoại và đáp ứng các rào cản kỹ thuật của thị trường quốc tế.
Với sự đồng hành của Chính phủ thông qua các chính sách ưu đãi và sự nỗ lực không ngừng của cộng đồng doanh nghiệp, ngành công nghiệp dược Việt Nam hoàn toàn có thể hiện thực hóa mục tiêu trở thành một trong những trung tâm sản xuất dược phẩm quan trọng của khu vực, đóng góp tích cực vào sự nghiệp chăm sóc sức khỏe nhân dân và sự hưng thịnh của nền kinh tế quốc gia trong thập kỷ tới.
10 Quy tắc Vàng trong Thực hành tốt sản xuất (GMP) Dược phẩm
Good Manufacturing Practices (GMP): 10 Nguyên tắc cốt lõi cần biết [Hướng dẫn 2026]







