Nhằm tiếp tục tăng cường hiệu lực, hiệu quả công tác quản lý nhà nước trong lĩnh vực dược, bảo đảm chất lượng thuốc, nguyên liệu làm thuốc và an toàn cho người sử dụng, Cục Quản lý Dược – Bộ Y tế xây dựng Kế hoạch đánh giá việc tuân thủ các nguyên tắc, tiêu chuẩn Thực hành tốt sản xuất thuốc (GMP) và Thực hành tốt phòng kiểm nghiệm thuốc (GLP) năm 2026.

Kế hoạch này được triển khai trên cơ sở các quy định hiện hành của pháp luật về dược, phù hợp với định hướng hội nhập quốc tế và yêu cầu nâng cao năng lực hệ thống đảm bảo chất lượng trong toàn ngành. Hoạt động đánh giá GMP, GLP không chỉ nhằm kiểm tra, giám sát việc tuân thủ của các cơ sở sản xuất, kiểm nghiệm mà còn góp phần hướng dẫn, hỗ trợ các đơn vị nâng cao năng lực, cải tiến hệ thống quản lý chất lượng theo tiêu chuẩn tiên tiến.
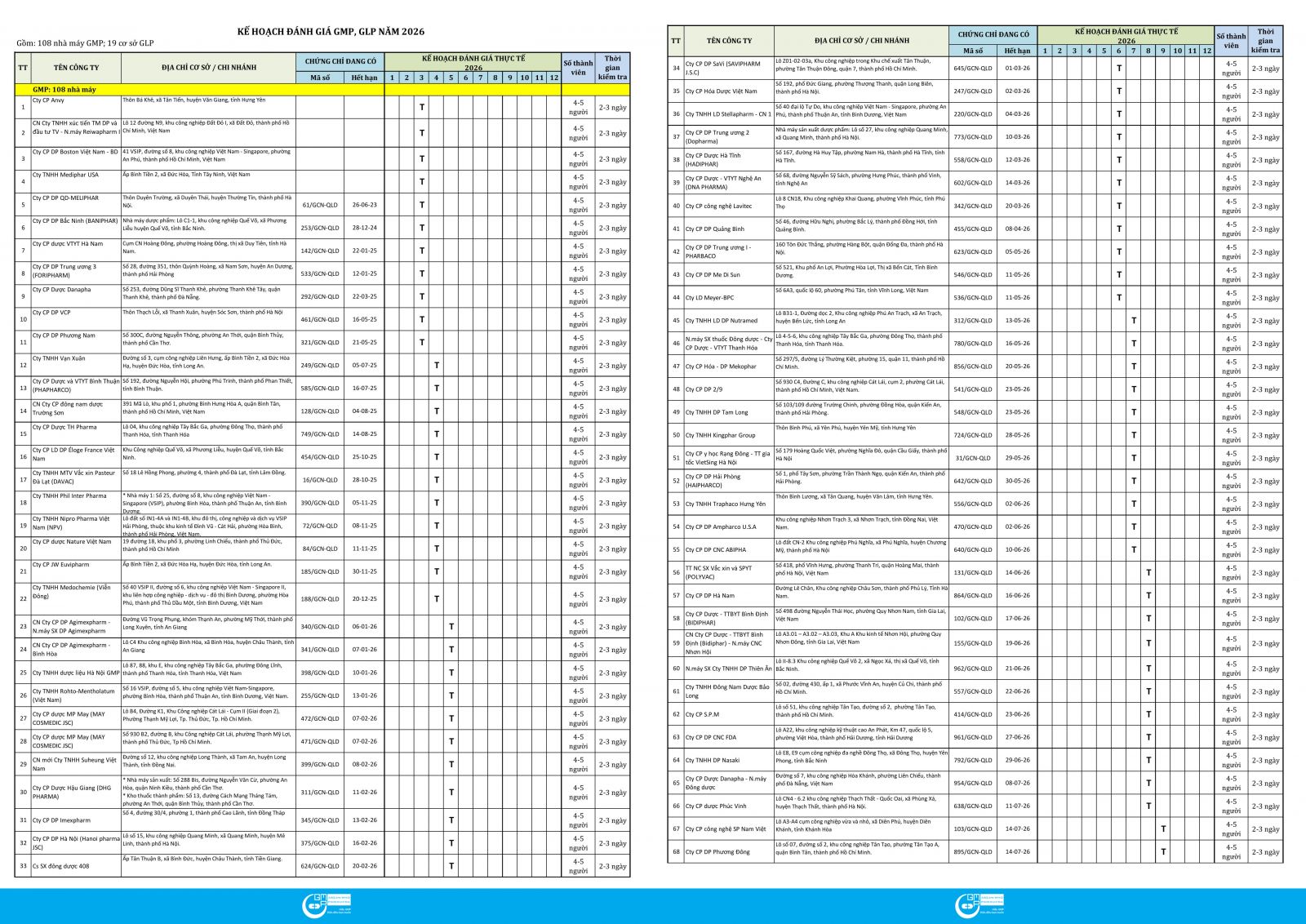
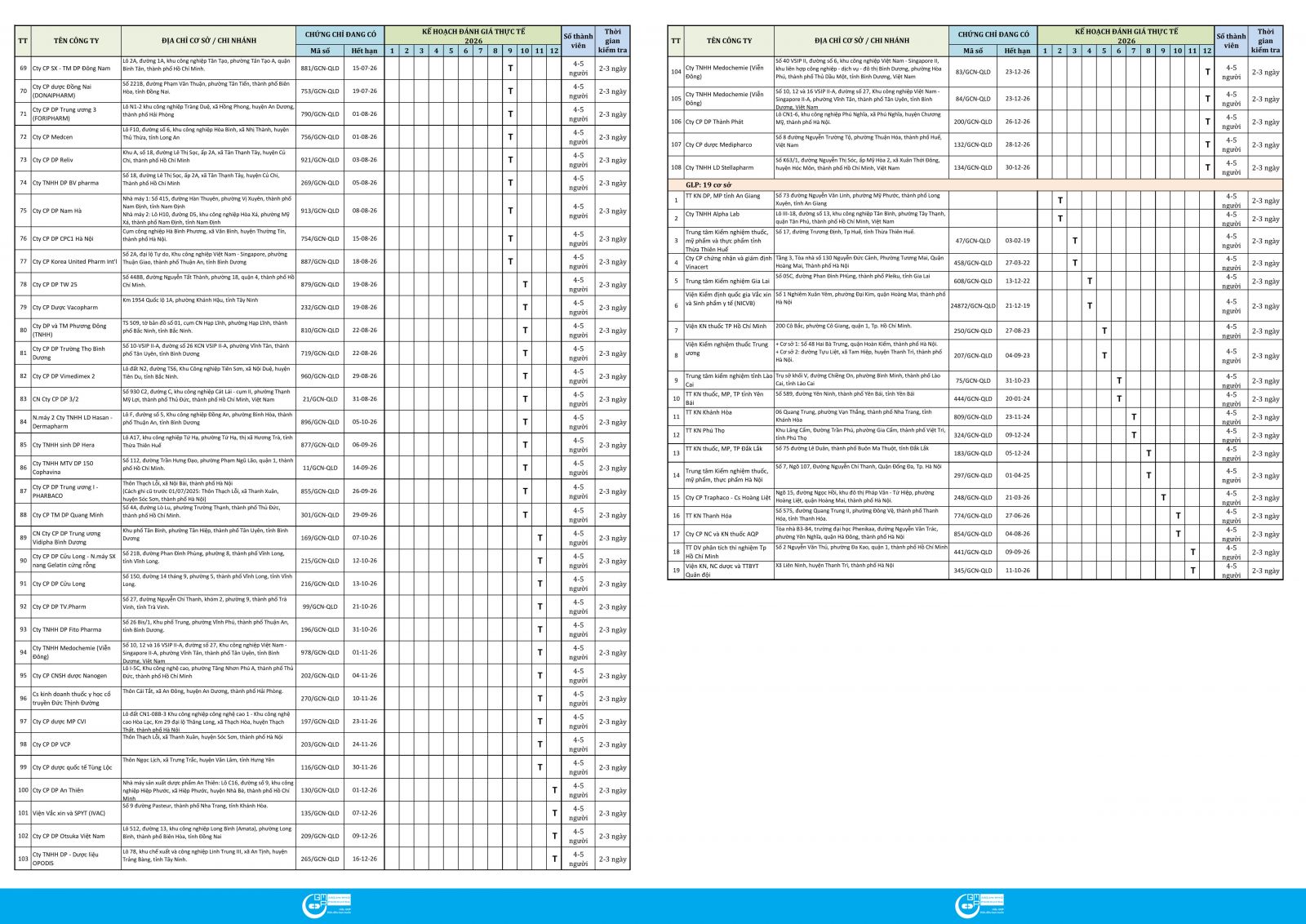
Thông qua việc triển khai Kế hoạch đánh giá GMP, GLP năm 2026, Cục Quản lý Dược hướng tới mục tiêu phát hiện, chấn chỉnh kịp thời các tồn tại, hạn chế; đồng thời khuyến khích các cơ sở áp dụng các thực hành tốt một cách bền vững, góp phần bảo đảm chất lượng thuốc lưu hành trên thị trường, đáp ứng nhu cầu chăm sóc và bảo vệ sức khỏe nhân dân.
Kế hoạch là căn cứ để các đơn vị liên quan tổ chức triển khai thực hiện đồng bộ, thống nhất, minh bạch và hiệu quả trong phạm vi toàn quốc.
>> Quý khách xem chi tiết kế hoạch đánh giá tại đây.






