1. Bối cảnh: Vì sao GACP được cắt giảm và đơn giản hóa?
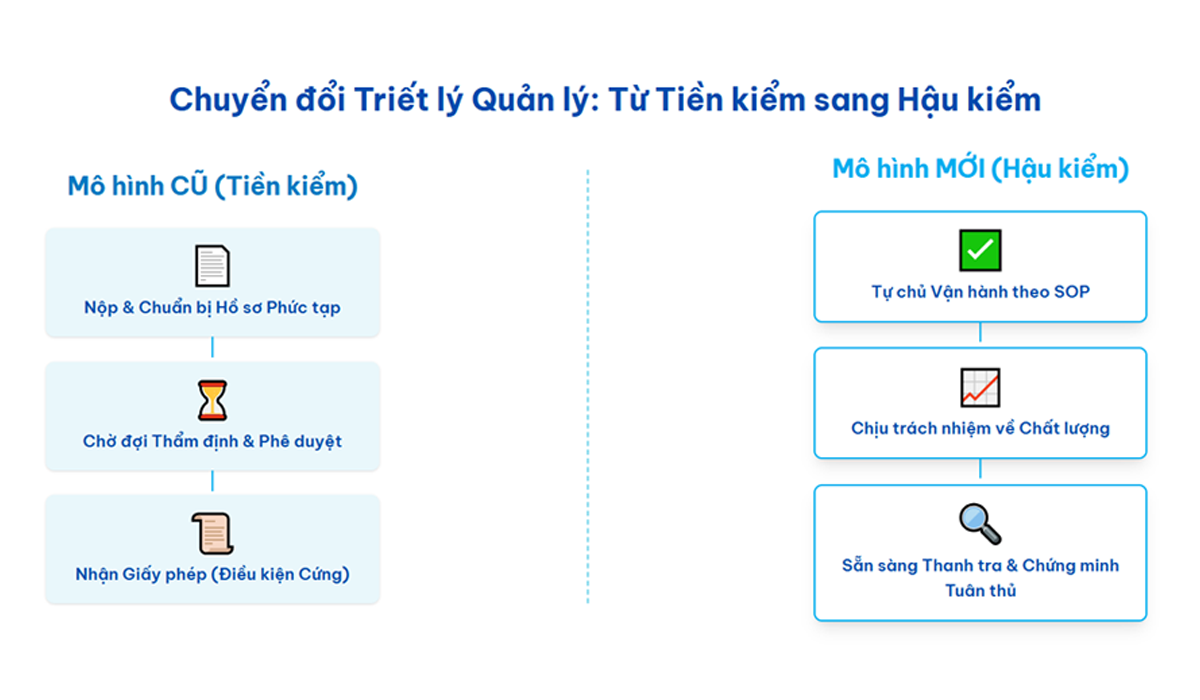
Tháng 3/2025, Chính phủ đã ban hành Nghị quyết số 66/NQ-CP với mục tiêu cắt giảm, đơn giản hóa thủ tục hành chính trong nhiều lĩnh vực, trong đó có quy định về "Thực hành tốt nuôi trồng và thu hái dược liệu" (GACP). Bộ Y tế đề xuất cắt giảm 14 điều kiện và đơn giản hóa 2 điều kiện kinh doanh liên quan đến GACP. Đây là sự chuyển đổi cách thức quản lý: từ việc kiểm soát "cách làm" sang tập trung vào "kết quả đầu ra". Doanh nghiệp được trao quyền tự chủ lớn hơn nhưng cũng phải chấp nhận trách nhiệm cao hơn trong việc đảm bảo chất lượng và an toàn của sản phẩm.
Xu hướng này phù hợp với định hướng cải cách tổng thể của Chính phủ nhằm tạo môi trường kinh doanh thuận lợi, giảm chi phí tuân thủ và nâng cao năng lực cạnh tranh quốc gia.
2. Tổng quan về GACP và tầm quan trọng đối với doanh nghiệp dược liệu
GACP (Good Agricultural and Collection Practices) - Thực hành tốt nuôi trồng và thu hái dược liệu là bộ tiêu chuẩn kỹ thuật do Tổ chức Y tế Thế giới (WHO) xây dựng nhằm hướng dẫn các doanh nghiệp và hộ sản xuất đảm bảo chất lượng, an toàn và hiệu quả của nguyên liệu dược liệu từ giai đoạn trồng trọt, thu hái, sơ chế đến bảo quản.
Mục tiêu của GACP là giúp kiểm soát rủi ro về chất lượng, an toàn, tránh nhiễm bẩn, đảm bảo đồng nhất và truy xuất nguồn gốc dược liệu. Đây là nền tảng quan trọng giúp doanh nghiệp xây dựng uy tín thương hiệu và gia tăng năng lực cạnh tranh trên thị trường.
Dù hiện nay Bộ Y tế Việt Nam đang đề xuất cắt giảm và đơn giản hóa các quy định liên quan đến GACP, việc áp dụng và duy trì chứng nhận GACP vẫn giữ vai trò then chốt, đặc biệt đối với các doanh nghiệp có định hướng mở rộng xuất khẩu. Các thị trường khó tính như EU, Mỹ, Nhật Bản vẫn yêu cầu các tiêu chuẩn cao hơn như GACP-WHO hay EU-GACP. Do đó, ngay cả trong bối cảnh cải cách GACP giúp giảm bớt thủ tục hành chính và chi phí tuân thủ, doanh nghiệp vẫn cần có tầm nhìn dài hạn để chủ động xây dựng hệ thống quản trị chất lượng bài bản, sẵn sàng cho mọi mục tiêu phát triển bền vững.
Xem thêm:Tổng quan về tiêu chuẩn GACP - WHO, Đảm bảo an toàn chất lượng riêng cho dược liệu
3. Những thay đổi nổi bật trong đề xuất cải cách GACP 2025
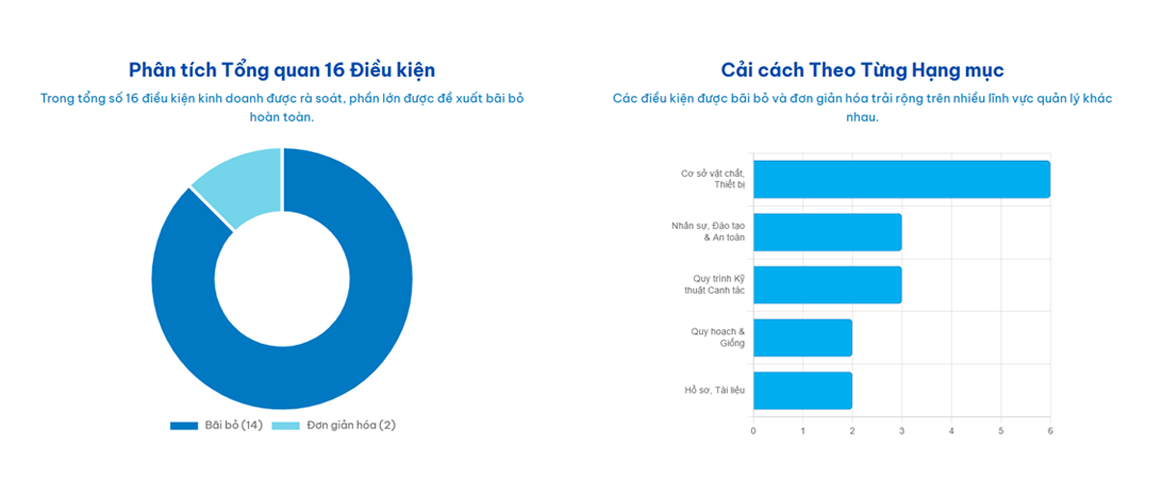
Dựa trên Dự thảo Quyết định của Thủ tướng Chính phủ năm 2025, những thay đổi quan trọng trong quy định GACP có thể chia thành 5 nhóm chính sau đây:
3.1. Quy hoạch, Giống và Môi trường Canh tác
Các quy định liên quan đến điều kiện vùng trồng và giống cây được bãi bỏ. Theo đó, yêu cầu vùng trồng phải phù hợp với sinh thái của cây dược liệu và việc giống phải sản xuất tập trung, cung ứng bởi đơn vị điều hành sẽ không còn bắt buộc. Điều này giúp doanh nghiệp có sự linh hoạt cao hơn trong tổ chức sản xuất.
3.2. Nhân sự, Đào tạo và An toàn Lao động
Các yêu cầu cụ thể về bố trí cán bộ chuyên môn, tổ chức tập huấn, đào tạo hằng năm, cũng như các quy định liên quan đến an toàn lao động trong quá trình vận hành thiết bị sẽ được bãi bỏ. Doanh nghiệp có thể chủ động xây dựng các chương trình đào tạo và quản lý nhân sự phù hợp với tình hình thực tế.
3.3. Quy trình Kỹ thuật Canh tác và Bảo vệ Thực vật
Nhóm quy định này tập trung vào việc đơn giản hóa quy trình kỹ thuật. Các yêu cầu về danh mục hóa chất, thuốc bảo vệ thực vật, cũng như quy định khoảng cách ly trước thu hoạch sẽ không còn là bắt buộc. Việc sử dụng hóa chất sẽ linh hoạt hơn, miễn là đảm bảo an toàn cho sản phẩm.
3.4. Cơ sở vật chất: Nhà xưởng, Kho bảo quản và Thiết bị
Nhiều quy định chi tiết liên quan đến thiết kế nhà xưởng, vật liệu xây dựng, kiểm soát nhiệt độ, độ ẩm, ánh sáng, cũng như quy trình bảo trì, bảo dưỡng sẽ được bãi bỏ. Doanh nghiệp sẽ không bị ràng buộc bởi các tiêu chí cứng nhắc mà chỉ cần đảm bảo sản phẩm cuối cùng đạt chất lượng yêu cầu. Việc kiểm nghiệm nước rửa và nước chiết xuất cũng được đơn giản hóa.
3.5. Quy trình Sau Thu hoạch và Hồ sơ Tài liệu
Các yêu cầu về việc lập hồ sơ đóng gói riêng và hồ sơ khắc phục khiếm khuyết sẽ được bãi bỏ. Thay vào đó, doanh nghiệp có thể tích hợp thông tin vào hệ thống hồ sơ tổng thể, giúp giảm bớt thủ tục và dễ dàng quản lý hơn.
Những điều chỉnh này phản ánh nỗ lực cải cách của cơ quan quản lý nhằm tạo môi trường kinh doanh thông thoáng hơn, đồng thời khuyến khích doanh nghiệp chủ động nâng cao năng lực quản trị chất lượng, phù hợp với mục tiêu phát triển bền vững của ngành dược liệu.
4. Chiến lược thích ứng khuyến nghị từ GMPc Việt Nam

Với vị thế là đơn vị tư vấn GMP/ GACP tiên phong và dẫn đầu tại Việt Nam, GMPc Việt Nam khuyến nghị các doanh nghiệp cần chủ động thực hiện các bước chiến lược sau:
4.1. Rà soát và nâng cấp hệ thống quản trị nội bộ (SOP, QMS)
- Xây dựng lại các Quy trình vận hành tiêu chuẩn (SOP) chi tiết, dễ áp dụng và phù hợp với thực tế.
- Duy trì chặt chẽ Hồ sơ lô, Hồ sơ đánh giá nội bộ làm cơ sở chứng minh tuân thủ khi bị thanh tra, kiểm tra.
- Đảm bảo hệ thống quản lý chất lượng (QMS) được vận hành thực chất chứ không chỉ dừng lại ở giấy tờ.
4.2. Chuyển đổi tư duy sang "sẵn sàng cho hậu kiểm"
- Thành lập hoặc củng cố bộ phận Đảm bảo chất lượng (QA) và Kiểm soát chất lượng (QC).
- Số hóa tài liệu và hồ sơ, xây dựng hệ thống lưu trữ khoa học để dễ dàng truy xuất khi cần thiết.
- Tạo văn hóa tuân thủ trong toàn bộ tổ chức, từ lãnh đạo đến nhân viên sản xuất.
4.3. Xây dựng chiến lược tuân thủ thông minh
- Với thị trường nội địa: Doanh nghiệp có thể áp dụng GACP theo phiên bản đơn giản hóa để tiết kiệm chi phí và tăng tính linh hoạt.
- Với thị trường xuất khẩu: Cần đầu tư hệ thống quản lý đạt chuẩn GACP-WHO, EU-GACP để đảm bảo khả năng cạnh tranh và mở rộng thị trường quốc tế.
4.4. Chủ động tham gia xây dựng chính sách
- Doanh nghiệp nên chủ động góp ý vào Dự thảo Thông tư sửa đổi thông qua các hiệp hội ngành nghề hoặc trực tiếp với cơ quan soạn thảo.
- Việc tham gia góp ý giúp đảm bảo chính sách phù hợp thực tiễn và giúp doanh nghiệp kịp thời chuẩn bị chiến lược ứng phó.

Với kinh nghiệm nhiều năm tư vấn và triển khai các tiêu chuẩn GMP, GACP, GACP-WHO, GMPc Việt Nam cam kết đồng hành cùng doanh nghiệp trên hành trình phát triển bền vững:
- Tư vấn thiết kế và xây dựng vùng trồng đạt chuẩn GACP, GACP-WHO.
- Hỗ trợ xây dựng hệ thống quản trị chất lượng nội bộ, chuẩn hóa SOP và hồ sơ lô.
- Đào tạo và nâng cao năng lực quản lý chất lượng và hậu kiểm.
- Cập nhật liên tục các quy định pháp lý và tiêu chuẩn quốc tế để giúp doanh nghiệp đi trước đón đầu.
Liên hệ ngay với chúng tôi để được hỗ trợ và tư vấn chi tiết về các tiêu chuẩn GMP/ GACP. Hotline 0982.866.668
Danh sách các dược liệu đã được đánh giá đạt cấp Giấy chứng nhận GACP (Tính đến ngày 20/02/2024)
Hướng dẫn thực hành tốt nuôi trồng dược liệu đạt tiêu chuẩn GACP WHO







