Trong cơ chế quản lý mới, việc sở hữu số tiếp nhận Phiếu công bố chỉ là bước khởi đầu của chu kỳ kiểm soát. Dự thảo Nghị định quản lý mỹ phẩm 2026 chuyển dịch trọng tâm sang công tác Hậu kiểm (Post-market Surveillance) nhằm thanh lọc thị trường. Đối với các chủ doanh nghiệp và quản lý nhà máy, việc thấu hiểu quy trình thanh tra thực địa và các kịch bản rủi ro là yếu tố sống còn để duy trì hoạt động kinh doanh bền vững.
Quý vị có thể tra cứu chi tiết danh mục các hành vi vi phạm tại: Quy định quản lý mỹ phẩm.
1. Cơ chế hậu kiểm dựa trên phân loại rủi ro sản phẩm
Dự thảo 2026 xác lập quy trình hậu kiểm hồ sơ và thực địa dựa trên tính chất của sản phẩm:
- Nhóm sản phẩm rủi ro thấp (Nhóm 1): Cơ quan quản lý sẽ hoàn thành việc kiểm tra hồ sơ hậu kiểm trong vòng 03 tháng kể từ ngày cấp số tiếp nhận.
- Nhóm sản phẩm rủi ro cao (Nhóm 2): Bao gồm các sản phẩm như làm trắng da, chống nắng, sản phẩm cho trẻ em... Nhóm này sẽ chịu sự giám sát chặt chẽ hơn về Phiếu kiểm nghiệm và báo cáo đánh giá an toàn ngay tại khâu thông quan hoặc xuất xưởng.
2. Quy trình thanh tra thực địa và yêu cầu đối ứng dữ liệu
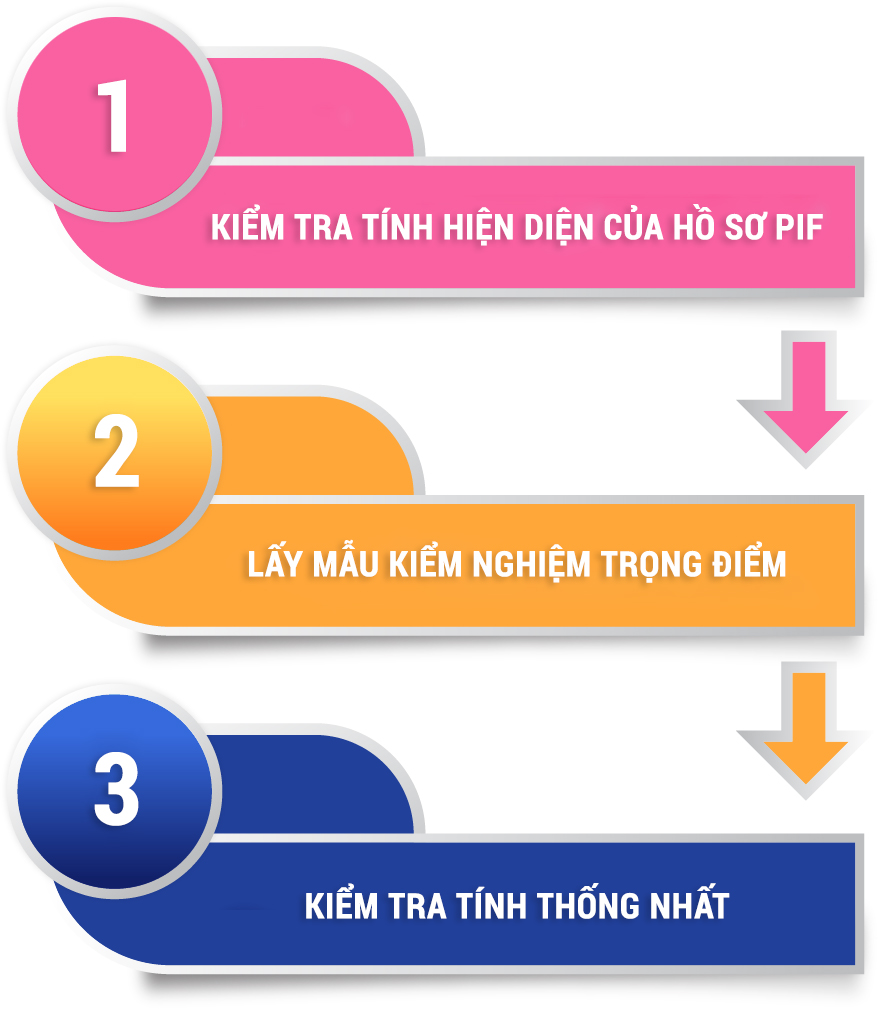
Khi có đoàn kiểm tra thực địa tại cơ sở sản xuất hoặc đơn vị chịu trách nhiệm đưa sản phẩm ra thị trường, doanh nghiệp phải tuân thủ nghiêm ngặt các mốc thời gian xuất trình dữ liệu:
- Kiểm tra tính hiện diện của Hồ sơ PIF: Như đã phân tích ở bài trước, Phần 1 của hồ sơ thông tin sản phẩm PIF phải có sẵn để đối chiếu ngay lập tức.
- Lấy mẫu kiểm nghiệm trọng điểm: Đoàn thanh tra có quyền lấy mẫu ngẫu nhiên trên thị trường hoặc tại kho thành phẩm để kiểm tra các chỉ tiêu giới hạn về kim loại nặng, vi sinh vật và các chất cấm (Annex).
- Kiểm tra tính thống nhất (Consistency Check): Đối chiếu sự tương thích giữa công thức ghi trên Phiếu công bố mỹ phẩm với hồ sơ lô sản xuất và kết quả kiểm nghiệm thực tế.
3. Các kịch bản rủi ro pháp lý và chế tài xử lý vi phạm
Dự thảo 2026 thiết lập khung hình phạt mang tính răn đe cao đối với các sai phạm chuyên môn:
- Thu hồi số tiếp nhận công bố: Áp dụng khi sản phẩm có công thức không đúng như hồ sơ đăng ký; nhãn ghi tính năng như thuốc; hoặc cơ sở không xuất trình được hồ sơ PIF đúng hạn.
- Ngừng tiếp nhận hồ sơ công bố (06 - 12 tháng): Hình phạt bổ sung đối với doanh nghiệp không thực hiện nghiêm túc việc thu hồi sản phẩm vi phạm hoặc có hành vi gian lận trong báo cáo an toàn.
- Công khai vi phạm: Thông tin về các sản phẩm không đạt chất lượng sẽ được đăng tải trực tuyến trên cổng thông tin của Bộ Y tế, gây ảnh hưởng trực tiếp đến uy tín thương hiệu.
4. Chiến lược quản trị rủi ro cho cấp quản lý nhà máy

Để đảm bảo nhà máy đạt chuẩn CGMP ASEAN luôn trong trạng thái sẵn sàng hậu kiểm, doanh nghiệp cần triển khai:
- Hệ thống cảnh báo sớm: Thiết lập quy trình tiếp nhận và xử lý phản hồi về biến cố có hại (Adverse Event). Đối với biến cố nghiêm trọng, phải báo cáo cơ quan quản lý trong vòng 07 ngày.
- Diễn tập hậu kiểm (Mock Audit): Định kỳ tổ chức các đợt tự kiểm tra hồ sơ và hiện trường nhà xưởng theo đúng checklist của Dự thảo 2026.
- Thẩm định nhà cung ứng nguyên liệu: Đảm bảo mọi nguyên liệu đầu vào đều có COA và MSDS chuẩn xác để phục vụ giải trình nguồn gốc khi có yêu cầu.
Kết luận từ chuyên gia GMPc Việt Nam
Hậu kiểm không phải là rào cản, mà là cơ chế bảo vệ các doanh nghiệp làm ăn chân chính. Một hệ thống quản trị rủi ro bài bản, bám sát quy định mỹ phẩm mới nhất sẽ giúp doanh nghiệp không chỉ vượt qua các đợt thanh tra mà còn khẳng định chất lượng vượt trội trên thị trường.
Mời quý vị xem thêm lộ trình chuyển tiếp cho các cơ sở sản xuất cũ đến hết năm 2027 tại: Tóm tắt thay đổi quy định mỹ phẩm 2026.







