Bộ KH&CN cho biết, theo xu hướng chung của thế giới, thị trường vaccine tại nước ta được dự báo là một thị trường lớn, có tốc độ phát triển cao trong những năm tới. Các nhà máy sản xuất vaccine trong nước được đầu tư nhiều hơn trong việc xây dựng đạt tiêu chuẩn, công nghệ sản xuất và bảo quản. Đặc biệt trong bối cảnh đại dịch COVID-19, Việt Nam đang từng bước tự chủ nguồn vaccine Covid -19, đưa vaccine Việt Nam tham gia thị trường quốc tế.
Vaccine Việt Nam sản xuất
Ngày 22/6/2015, Việt Nam đã chính thức trở thành quốc gia thứ 39 được Tổ chức Y tế Thế giới (WHO) công nhận đạt Tiêu chuẩn Cơ quan Quản lý Quốc gia về vaccine (NRA). Với giấy chứng nhận này, Việt Nam có đủ khả năng giám sát, đánh giá chất lượng vaccine một cách độc lập. Là một trong 42 quốc gia có thể sản xuất được vắc xin trên thế giới, vaccine của Việt Nam làm ra có thể xuất khẩu ra thế giới và các nước công nghệ cao có thể yên tâm đầu tư vào Việt Nam cùng hợp tác sản xuất vắc-xin.
Với định hướng chuyển hóa các thành tựu khoa học trong lĩnh vực vaccine thành hàng hóa có giá trị thương mại cao, đáp ứng yêu cầu của thị trường trong nước và xuất khẩu, Bộ Y tế đã đề xuất nâng vaccine phòng bệnh cho người thành sản phẩm quốc gia và đã được Chính phủ chấp thuận. Theo đó, khoảng đến năm 2020, nước ta sẽ sản xuất và thương mại hóa được ít nhất 7 loại vaccine quan trọng phòng bệnh cho người (vaccine đa giá 5 trong 1 và 6 trong 1, vaccine Rota, viêm não Nhật Bản, cúm mùa, thương hàn, dại và viêm gan A), đáp ứng đủ yêu cầu chương trình tiêm chủng mở rộng trong nước, thay thế vaccine nhập khẩu, tiến tới xuất khẩu vaccine ra một số nước trong khu vực và trên thế giới.

Trên thực tế, Việt Nam đã đạt được nhiều kết quả đáng khích lệ, cụ thể:
- Hiện tại, Việt Nam đã tự sản xuất hầu như toàn bộ 11 loại vắc-xin, cung cấp đủ cho chương trình TCMR, như: Bạch hầu, Ho gà, Uốn ván, Bại liệt uống, Sởi, Thương hàn, Viêm gan B, Lao, Viêm não Nhật Bản, Tả uống. Đặc biệt, từ tháng 4/2018, vaccine Sởi - Rubella (MRVAC) do Việt Nam sản xuất đã được sử dụng trên quy mô toàn quốc cho trẻ từ 18 tháng tuổi trong TCMR.
- Việt Nam đã triển khai nhiều dự án sản xuất vaccine phù hợp với khuyến cáo của WHO và đang tích cực nghiên cứu và tự sản xuất thêm các loại vaccine nhằm bảo vệ trẻ em. Trong đó, Viện Vaccine và sinh phẩm y tế được giao thực hiện Dự án “Vaccine nghiên cứu phát triển sản phẩm vaccine cúm mùa”, phòng 3 chủng cúm cơ bản là A/H1N1, A/H3N2 và cúm B và Dự án “Nghiên cứu sản xuất vaccine phối hợp 5 trong 1 hấp thụ, dạng dung dịch”. Trong thời gian tới, Viện dự kiến sẽ tự sản xuất được vaccine 5 trong 1 (phòng các bệnh bạch hầu, ho gà, uốn ván, viêm gan B và Hib). VABIOTECH cũng đang triển khai Dự án “Nghiên cứu phát triển sản phẩm vaccine viêm não Nhật Bản trên tế bào Vero. VABIOTECH đang chuẩn bị hồ sơ xin đăng ký lưu hành vaccine viêm não Nhật Bản trên tế bào Vero (JECEVAC) tại Việt Nam.
- Đối với vaccine COVID-19, Việt Nam hiện có 4 đơn vị tham gia nghiên cứu, sản xuất vaccine COVID-19 là Công ty TNHH MTV Vaccine và Sinh phẩm số 1 (VABIOTECH); Trung tâm Nghiên cứu Sản xuất Vaccine và Sinh phẩm Y tế (POLYVAC); Viện Vaccine và Sinh phẩm y tế (IVAC) và Công ty TNHH Dược Nanogen (NANOGEN).
- Việt Nam hiện có 2 vaccine Covid-19 "made in Việt Nam" bao gồm NANOCOVAX của NANOGEN sản xuất, vaccine COVIVAC của IVAC đang được thử nghiệm lâm sàng. Vaccine NANOCOVAX đã hoàn thành thử nghiệm lâm sàng giai đoạn 1 và sẽ tiếp tục triển khai giai đoạn 2 ngay trong đầu tháng 2/2021 tới. Vaccine COVIVAC của IVAC đã được khởi động thử nghiệm giai đoạn 1 ngày 21/1/2021 và dự kiến kết thúc vào cuối tháng 2/2021 để tiếp tục triển khai giai đoạn 2 trong tháng 3/2021.
Vaccine nhập khẩu
- Bên cạnh các loại vaccine đã sản xuất được ở Việt nam, hiện vẫn có nhiều loại vaccine vẫn phải nhập khẩu như các loại vaccine 5 trong 1 & 6 trong 1.
- Vaccine chủ yếu được nhập từ các nước phát triển và từ các đối tác lớn trên thế giới. Lượng vaccine nhập khẩu ước tính chiếm khoảng 30% tổng sản lượng.
Nhu cầu chung về vaccine các loại
- Thống kê dân số Việt nam đến năm 2020 đạt khoảng 97.3 triệu người, trong đó dưới 15 tuổi khoảng 25 triệu người, từ trên 15 đến 64 tuổi khoảng 66 triệu và trên 64 tuổi khoảng 6 triệu người.
- Theo số liệu thống kê, hiện có trên 95% trẻ mới sinh được tiêm phòng theo chương trình TCMR, trên 60% được tiêm phòng nâng cao hoặc các mũi 5 trong 1 hoặc 6 trong một. Ước tính tổng cộng khoảng 6 triệu liều/năm cho trẻ mới sinh.
- Các trẻ từ 1-5 tuổi còn được tiếp tục tiêm phòng các bệnh khác các mũi nhắc lại. Ngoài ra, cũng có một lượng những người trên 5 tuổi tiêm phòng bổ xung các bệnh khác. Ước tính tổng cộng khoảng 24 triệu liều/năm.
- Tổng nhu cầu tiêm phòng thường xuyên 1 năm dự kiến khoảng 30 triệu liều (không kể các phát sinh như tiêm phòng Covid 19).
- Lượng sử dụng trung bình khoảng 2,5 triệu liều/tháng, trong đó khoảng 70% là vaccine sản xuất trong nước và khoảng 30% là vaccine nhập khẩu.
- Thời hạn lưu trữ vaccine được khoảng 6 tháng, nhưng vaccine thường được sản xuất/nhập khẩu, lưu kho một thời gian ngắn rồi phân phối về các kho trung gian và chuyển đến các điểm tiêm phòng. Vì vậy ước tính thời gian lưu kho của vaccine trung bình chỉ khoảng 2 tháng. Lượng kho tập trung ở 2 miền cần để lưu trữ vaccine ước tính khoảng 5 triệu liều tương đương khoảng 25m3 net, khoảng 50m3 kho lạnh.
Nhu cầu về vaccine Covid 19
- Đây là loại vaccine đặc thù, nhưng chỉ mang tính chất mùa vụ. Dự kiến Việt Nam sẽ mua và nhập khẩu khoảng 150 triệu liều vaccine trong khoảng thời gian từ năm 2021 đến 2022.
- Trong đó dự kiến sẽ có khoảng 20-30% cần bảo quản ở nhiệt độ -70oC, còn lại chỉ cần bảo quản ở nhiệt độ -18oC đến 8oC như các vaccine thông thường khác.
- Vaccine dự kiến được nhập khẩu từ nhiều nguồn và nhiều nước khác nhau, ước tính khoảng 50% số lượng được nhập về sân bay Nội bài và 50% nhập về sân bay Tân sơn nhất.
- Tính đến ngày 28/3/2021, Hải Dương có số người được tiêm liều vắc xin COVID-19 cao nhất Việt Nam với hơn 18 nghìn người được tiêm. Trong khi đó, tại Hà Nội có 7,6 nghìn người được tiêm vắc xin COVID-19. Việt Nam bắt đầu chiến dịch tiêm chủng COVID-19 vào đầu tháng 3 năm 2021, với vắc xin AstraZeneca là vắc xin đầu tiên được sử dụng cho các nhân viên y tế tuyến đầu.
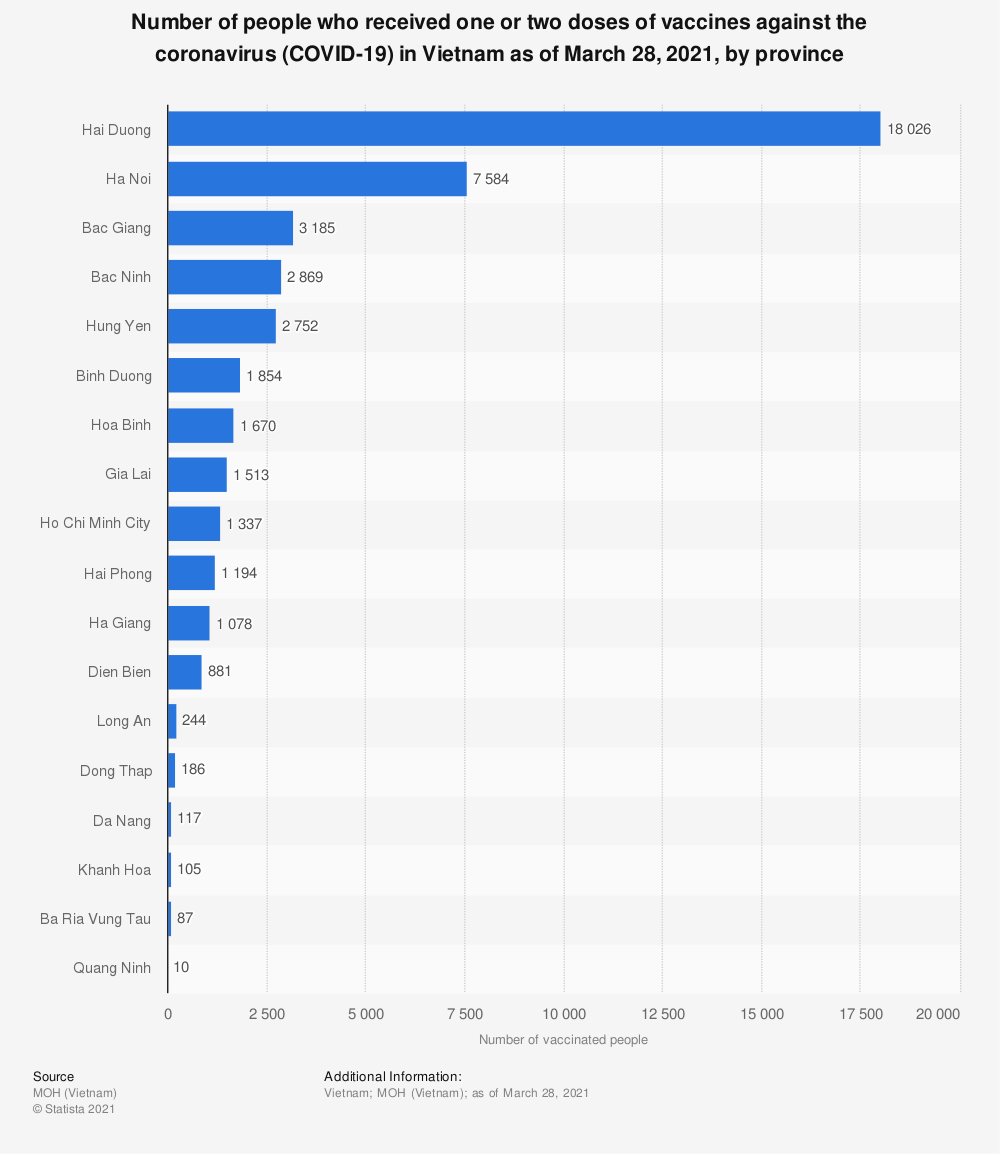
Số người đã tiêm một hoặc hai liều vắc xin phòng chống vi rút coronavirus (COVID-19) ở Việt Nam tính đến ngày 28 tháng 3 năm 2021, theo tỉnh
- Vaccine được lưu trữ tối đa 6 tháng, nhưng thời gian lưu trữ trung bình chỉ khoảng 2 tháng. Với lượng vaccine Covid 19 nhập khẩu dự kiến nêu trên, tổng lượng vaccine Covid lưu tại tổng kho tại Miền Bắc và Miền Nam tại một thời điểm tối đa khoảng 12,5 triệu liều, chia đều cho 2 miền. Như vậy công suất tổng kho lưu vaccine Covid 19 tại mỗi miền cần khoảng 6,25 triệu liều, tương đương thể tích net khoảng 32m3, cộng theo bao bì thì thể tích lưu trữ lạnh khoảng 64m3.
- Trong đó vaccine dược lưu tại tổng kho, các kho trung gian và tại cả các cơ sở y tế. Hạ tầng hiện tại của các đơn vị nhập khẩu & phân phối vaccine về cơ bản đã đáp ứng được nhu cầu. Khoảng 20-30% trong đó có thể cần bảo quản lạnh sâu (-70oC), chiếm thể tích khoảng 10m3, tương đương khoảng 10 tủ lạnh sâu có dung tích 950L.
GMPC Việt Nam là Công ty tư vấn hàng đầu hoạt động trong lĩnh vực tư vấn Đầu tư - Thiết kế - Xây dựng - Vận hành các Nhà máy sản xuất tuân thủ theo các nguyên tắc, tiêu chuẩn GMP (WHO, EU, ASEAN, HS) cho các lĩnh vực: Sản xuất Dược phẩm, Mỹ phẩm, Thực phẩm bảo vệ sức khỏe (TPCN)...
Trong lĩnh vực tư vấn nhà máy sản xuất vaccine, GMPC Việt Nam tự tin khi có thể đem đến cho quý doanh nghiệp giải pháp tổng thể từ tư vấn, thiết kế dây chuyền sản xuất, nhà máy cho đến thi công lắp đặt, hoàn thiện hồ sơ GMP cho doanh nghiệp. Chúng tôi đã giúp đỡ rất nhiều doanh nghiệp Dược phẩm xây dựng nhà máy đạt chuẩn như: Dược hậu Giang, Mediplantex, CVI, Viện nghiên cứu hạt nhân, Viện dược liệu,…

Tư vấn xây dựng nhà máy sản xuất vaccine đạt chuẩn GMP
Chúng tôi luôn đưa các giải pháp tư vấn Đơn giản hóa - Tối ưu chi phí - Đảm bảo đạt chứng nhận cho nhà máy sản xuất Vaccine đạt chuẩn GMP bao gồm
1. Lập Báo cáo Dự án đầu tư
2. Tư vấn Công nghệ và Thiết bị
3. Thiết kế bản vẽ thi công chi tiết
4. Quản lý Dự án - Giám sát thi công
5. Đào tạo, Hướng dẫn thực hành
6. Lập hồ sơ đánh giá GMP
7. Tư vấn tái đánh giá GMP
Chúng tôi mong đợi có cơ hội được đóng góp kinh nghiệm và hiểu biết của mình trong Dự án nhà máy sản xuất vaccine của Quý vị.
Thông tin liên hệ:
CÔNG TY CỔ PHẦN GMPC VIỆT NAM
• Trụ sở chính (Hà Nội): Blue Office, số 4- BT1- phố Bùi Xuân Phái- phường Mỹ Đình 2- quận Nam Từ Liêm
• Tel: 0243.787.2242 | CEO hotline: 0982.866.668
• Email: contact@gmp.com.vn
• VPĐD tại thành phố Hồ Chí Minh: Lầu 2 – Số 156/1/1 Cộng Hòa, Phường 12, Quận Tân Bình
• Tel: 0283.811.7383







